
【题目】设NA表示阿伏伽德罗常数的值,下列说法正确的是:
A. 同温同压下,3molO2和2molO3,它们的密度比为 1:1
B. 46 克NO2和N2O4 的混合气体原子个数为3NA
C. 生成7.1gCl2 转移电子数目为0.2NA
D. 标准状况下,11.2LSO3所含的原子个数为2NA
科目:高中化学 来源: 题型:
【题目】根据所学知识填空
(1)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料.已知:SeO2在常温下是白色的晶体,熔点为340﹣350℃,则SeO2晶体属于晶体,SeO2中Se原子采取的杂化类型为
(2)卤素单质及其化合物在工农业生产和生活中都有重要的用途.
①同主族元素的电负性大小存在一定的规律,卤族元素(F、Cl、Br、I)中,电负性最小的是 , 基态Br原子的价电子排布为 .
②硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3NH3 . BF3分子的分子构型为 , BF3NH3中BF3与NH3之间通过结合(填“离子键”、“配位键”或“氢键”).
(3)某金属是抗癌药物中的明星元素,其晶体中金属原子的堆积方式如图所示.该晶胞中金属原子的配位数为 , 若已知金属的摩尔质量为Mg/mol,原子半径为rpm,阿伏加德罗常数为NA , 则该晶胞的密度为g/cm3 . (用含M、NA、则的代数式表示,1pm=1.0X10﹣10cm) 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①海带等藻类物质经过处理后,可以得到碘水,向碘水中加入四氯化碳以提取碘单质的实验操作叫________,该操作需要的玻璃仪器有________。
②某NaCl样品中可能含有SO42-,CO32-,为检验杂质离子的存在,采取如下实验步骤:样品![]() 无明显现象
无明显现象![]() 无明显现象。则加入的试剂A为_______,B为_______,该现象证明样品中不含有____。
无明显现象。则加入的试剂A为_______,B为_______,该现象证明样品中不含有____。
③在后续实验中需要使用450mL0.5 mol·L- 1NaCl溶液,为配制该浓度NaCl溶液进行实验,需用托盘天平称取NaCl_______g。配制NaCl溶液时,若出现下列操作,会使配制浓度偏高的是(_____)
A.天平砝码己锈蚀 B.配制过程中未用蒸馏水洗涤烧杯和玻璃棒
C.转移溶液时有溶液溅出 D.定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是﹣285.8kJmlo﹣1﹣1411.0kJmlo﹣1和﹣1366.8kJmlo﹣1 , 则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
A.﹣44.2kJmol﹣1
B.+44.2kJmol﹣1
C.﹣330kJmol﹣1
D.+330kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.下列叙述错误的是( ) 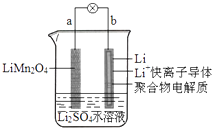
A.a为电池的正极
B.电池放电反应为LiMn2O4=Li1﹣xMn2O4+xLi
C.放电时,a极锂的化合价不发生变化
D.放电时,溶液中的Li+从b向a迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大.X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素.
回答下列问题:
(1)L的元素符号为;M在元素周期表中的位置为;五种元素的原子半径从大到小的顺序是(用元素符号表示).
(2)Z、X两元素按原子数目比l:3和2:4构成分子A和B,A的电子式为 , B的结构式为 .
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为 , 其最高价氧化物对应的水化物化学式为 . 该族2~5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol硒化氢反应热的是(填字母代号).
a.+99.7molL﹣1 b.+29.7molL﹣1 c.﹣20.6molL﹣1 d.﹣241.8kJmol﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的AlCl3 溶液中逐滴加入NaOH溶液,生成沉淀Al(OH)3的量随NaOH加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( ) 
A.a点对应的溶液中:K+、NH4+、I﹣、CO32﹣
B.b点对应的溶液中:Na+、H+、S2﹣、Cl﹣
C.c点对应的溶液中:NH4+、H+、NO3﹣、SO42﹣
D.d点对应的溶液中:Na+、K+、SO42﹣、HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,前者无法决定后者的是
A.原子的核外电子排布----元素的金属性强弱
B.化合物的内在结构----电解质的相对强弱
C.反应温度的高低----化学平衡的移动程度
D.反应物的化学性质----化学反应速率的快慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com