
【题目】聚对苯二甲酸乙二醇酯(PET),俗称涤纶树脂,是一种重要的有机高分子材料。其结构为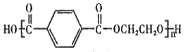 。利用有机物A合成PET的路线如图。
。利用有机物A合成PET的路线如图。
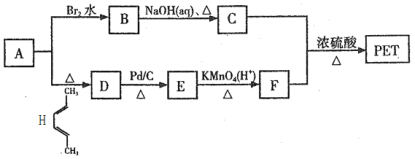
已知:①![]() ;②
;②![]() 。
。
根据题意回答下列问题:
(1)A的名称是_______,C中所含官能团的名称是______。
(2)H在一定条件下发生加聚反应生成顺式产物的结构简式___________。
(3)A→D、B→C的反应类型分别为______、______。
(4)写出C+F→PET的化学反应方程式________。
(5)G是F的同系物,其相对分子质量比F多28,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,则符合该条件的G的同分异构体共有___种,写出其中2种的结构简式______。
(6)参照上述合成路线,以1,3-丁二烯为原料经3步制得丁苯橡胶。(无机试剂任选)
![]()
![]() I
I![]()
![]()
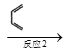
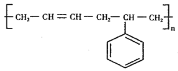
I的结构简式为_____;反应1的条件为_____;反应2的反应类型为_____。
【答案】乙烯 羟基 ![]() 加成反应 取代反应 n
加成反应 取代反应 n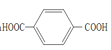 +nHOCH2CH2OH
+nHOCH2CH2OH![]()
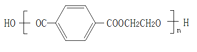 +(2n-1)H2O 4
+(2n-1)H2O 4 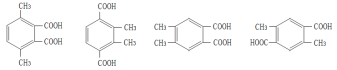 (任意2种)
(任意2种) ![]() Pd/C,加热 加聚反应
Pd/C,加热 加聚反应
【解析】
根据聚对苯二甲酸乙二醇酯(PET)的结构![]() 可知,C、F是乙二醇和对苯二甲酸,根据生成C和F的条件可知,C为乙二醇,F为对苯二甲酸,则B为1,2-二溴乙烷,A为乙烯;根据已知信息,乙烯与
可知,C、F是乙二醇和对苯二甲酸,根据生成C和F的条件可知,C为乙二醇,F为对苯二甲酸,则B为1,2-二溴乙烷,A为乙烯;根据已知信息,乙烯与![]() 反应生成D,D为
反应生成D,D为![]() ,E为对二甲苯。据此解答。
,E为对二甲苯。据此解答。
(1)根据上述分析,A为乙烯,C为乙二醇,所含官能团为羟基,故答案为:乙烯;羟基;
(2)H为![]() ,在一定条件下发生加聚反应生成顺式产物的结构简式为
,在一定条件下发生加聚反应生成顺式产物的结构简式为![]() ;
;
(3)根据上述分析,A→D为加成反应、B→C为卤代烃的水解反应,属于取代反应,故答案为:加成反应;取代反应(或水解反应);
(4)C+F→PET的化学反应方程式为n +nHOCH2CH2OH
+nHOCH2CH2OH![]()
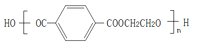 +(2n-1)H2O;
+(2n-1)H2O;
(5)G是F(![]() )的同系物,其相对分子质量比F多28,多2个甲基,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,即6:2:2,则符合该条件的G的同分异构体有:
)的同系物,其相对分子质量比F多28,多2个甲基,G的核磁共振氢谱有三组峰,峰面积比为3:1:1,即6:2:2,则符合该条件的G的同分异构体有: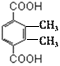 、
、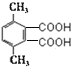 、
、 、
、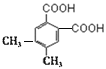 ,共4种;
,共4种;
(6)以1,3-丁二烯为原料制备丁苯橡胶( )。根据已知信息,首先需要制备苯乙烯,可以由2分子1,3-丁二烯发生加成反应生成
)。根据已知信息,首先需要制备苯乙烯,可以由2分子1,3-丁二烯发生加成反应生成![]() ,再由
,再由![]() 制备苯乙烯,最后苯乙烯与1,3-丁二烯发生加聚反应生成丁苯橡胶,合成路线为
制备苯乙烯,最后苯乙烯与1,3-丁二烯发生加聚反应生成丁苯橡胶,合成路线为 ,故I的结构简式为
,故I的结构简式为![]() ;反应1的条件为Pd/C,加热;反应2的反应类型为加聚反应。
;反应1的条件为Pd/C,加热;反应2的反应类型为加聚反应。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.235g核素![]() U发生裂变反应:
U发生裂变反应:![]() +
+![]()
![]()
![]() Sr+
Sr+![]() Xe+10
Xe+10![]() ,净产生的中子(
,净产生的中子(![]() )数为10NA
)数为10NA
B.![]() Cl与
Cl与![]() Cl得电子能力相同
Cl得电子能力相同
C.中子数为146、质子数为92的铀(U)原子:![]() U
U
D.![]() U和
U和![]() U是中子数不同,质子数相同的同种核素
U是中子数不同,质子数相同的同种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国由海水提取的食盐(海盐)不足四成,大部分产自内陆盐湖(湖盐)和盐矿(矿盐)。
(1)由内陆盐湖水为原料进行晒盐,有“夏天采盐(食盐)、冬天捞硝(芒硝)”的说法,下列对其化学原理的描述正确的是___(选填编号)。
a.由夏到冬,芒硝的溶解度变小
b.由冬到夏,氯化钠的溶解度变小
c.夏天温度高,氯化钠易结晶析出
(2)芒硝型矿盐卤水中含有一定量Na2SO4和少量Ca2+、Mg2+、H2S等杂质,利用硫酸钙微溶于水的性质,用石灰-烟道气(CO2)法净化芒硝型矿盐卤水的流程如图:
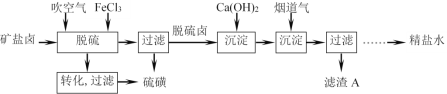
脱硫工序中先吹空气,发生物理和化学变化:物理变化是氢硫酸有挥发性,部分被直接吹出,化学变化是___(用化学方程式表示)。再加入稍过量的FeCl3溶液除去残留的硫化氢。检验FeCl3已经过量的试剂是___(填写化学式)。
(3)加入Ca(OH)2能降低芒硝浓度并生成烧碱,同时除去Fe3+,另一目的是___。滤渣A的主要成分除了Fe(OH)3外,还有___(填写化学式)。
(4)如图所示是石灰-纯碱法净化芒硝型矿盐卤水的部分流程:加入纯碱的作用是___(选填编号)。
a.调节溶液的pH b.除去溶液中的Ca2+
c.除去溶液中的Mg2+ d.除去溶液中的SO42―
石灰-烟道气法与石灰-纯碱法相比较,石灰-烟道气法的优点是___。

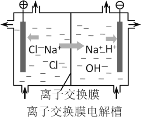
(5)如图是离子交换膜法电解食盐水的示意图,离子交换膜只允许阳离子通过,上述精盐水需要进行二次精制后才能作为离子交换膜电解槽的原料。对盐水进行二次精制的目的是___(选填编号)。
a.进一步降低Ca2+、Mg2+的浓度,提高烧碱纯度
b.进一步降低SO42―的浓度,提高烧碱纯度
c.防止杂质离子与碱生成的沉淀堵塞离子交换膜
d.防止溶液酸性或碱性过强,腐蚀离子交换膜
盐水中硫酸根浓度过高会使生成的氯气中混有氧气,检验氯气中是否含有少量氧气的操作是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室从海带中提取碘,设计实验流程如下:
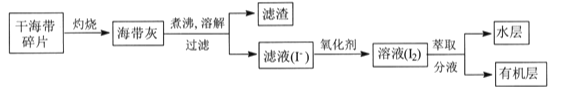
下列说法错误的是
A.过滤操作主要除去海带灰中难溶于水的固体,它们主要是无机物
B.氧化剂参加反应的离子方程式为2I-+H2O2+2H+=I2+2H2O
C.萃取过程所用有机溶剂可以是酒精或四氯化碳
D.因I2易升华,I2的有机溶液难以通过蒸馏法彻底分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A的分子式为C8H8O2。A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱和核磁共振氢谱如图。下列关于A的说法中不正确的是( )
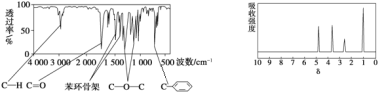
A. 与A属于同类化合物的同分异构体只有3种
B. 符合题中A分子结构特征的有机物只有1种
C. A在一定条件下可与3molH2发生加成反应
D. A分子属于酯类化合物,在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸乙酯可由苯甲酸与乙醇在浓硫酸共热下反应制得,反应装置如图(部分装置省略),反应原理如下:
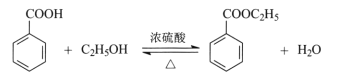
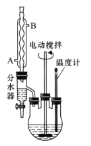
实验操作步骤:
①向三颈烧瓶内加入12.2g苯甲酸、25mL乙醇、20mL苯及4mL浓硫酸,摇匀,加入沸石。
②装上分水器、电动搅拌器和温度计,加热至分水器下层液体接近支管时将下层液体放入量筒中。继续蒸馏,蒸出过量的乙醇,至瓶内有白烟(约3h),停止加热。
③将反应液倒入盛有80mL冷水的烧杯中,在搅拌下分批加入碳酸钠粉末至溶液无二氧化碳逸出,用pH试纸检验至呈中性。
④用分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层。用无水CaC12干燥,粗产物进行蒸馏,低温蒸出乙醚。当温度超过140℃时,直接接收210-213℃的馏分,最终通过蒸馏得到纯净苯甲酸乙酯12.8mL。
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
苯甲酸 | 122 | 1.27 | 249 | 微溶于水,易溶于乙醇、乙醚 |
苯甲酸乙酯 | 150 | 1.05 | 211-213 | 微溶于热水,溶于乙醇、乙醚 |
乙醇 | 46 | 0.79 | 78.5 | 易溶于水 |
乙醚 | 74 | 0.73 | 34.5 | 微溶于水 |
回答以下问题:
(1)反应装置中分水器上方的仪器名称是______,其作用是____
(2)步骤①中加浓硫酸的作用是_________,加沸石的目的是______。
(3)步骤②中使用分水器除水的目的是_________。
(4)步骤③中加入碳酸钠的目的是________ 。
(5)步骤④中有机层从分液漏斗的____(选填“上口倒出”或“下口放出”)。
(6)本实验所得到的苯甲酸乙酯产率是________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
①盐卤(含MgCl2)![]() Mg(OH)2
Mg(OH)2![]() MgCl2溶液
MgCl2溶液![]() 无水MgCl2
无水MgCl2
②铝土矿![]() AlO2-
AlO2-![]() Al(OH)3
Al(OH)3![]() Al2O3
Al2O3
③NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
④NaCl溶液![]() Cl2
Cl2![]() 无水FeCl2
无水FeCl2
⑤S![]() SO3
SO3![]() H2SO4
H2SO4
⑥SiO2![]() Na2SiO3溶液
Na2SiO3溶液![]() H2SiO3
H2SiO3
A. ①③⑥B. ③⑤⑥C. ①④⑤D. ③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见的A~J物质存在如下转化关系示意图(反应条件已略去),已知通常情况下A、H为固态金属单质,B、D为气态非金属单质,E为淡黄色固体,F为无色液体,J为红褐色沉淀。请回答下列问题:

(1)写出下列物质的化学式:H________;D__________。
(2)写出下列转化的化学方程式或离子方程式:
①E+F→D+G的化学方程式:__________________________________;
②G+I→C+J的离子方程式:_________________________________。
(3)若要检验I物质的阳离子所加入的试剂是________________________。实验现象为:___________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组以Mg(NO3)2为研究对象,拟通过实验初步探究硝酸盐热分解的规律。
(提出猜想)小组提出如下4种猜想:
甲:Mg(NO2)2、NO2、O2 乙:MgO、NO2、O2
丙:Mg3N2、O2 丁:MgO、NO2、N2
(1)查阅资料得知,NO2可被NaOH溶液吸收,反应的化学方程式为:_________。
(2)实验前,小组成员经讨论认定猜想丁不成立,理由是________。
(实验操作)
(3)设计如图装置,用氮气排尽装置中空气,其目的是_______;加热Mg(NO3)2固体,AB装置实验现象是:________,说明有Mg(NO3)2固体分解了,有NO2生成。

(4)有同学提出可用亚硫酸钠溶液检验是否有氧气产生,但通入之前,还需在BD装置间增加滴有酚酞的氢氧化钠溶液,其作用是:_______。
(5)小组讨论后认为即便通过C后有氧气,仅仅用亚硫酸钠溶液仍然难以检验,因为:______,改进的措施是可在亚硫酸钠溶液中加入_______。
(6)上述系列改进后,如果分解产物中有O2存在,排除装置与操作的原因,未检测到的原因是______。(用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com