
(10分)N2在化工生产、农业、医疗、航天航空等领域用途广泛。现提供以下装置(连接仪器略去):
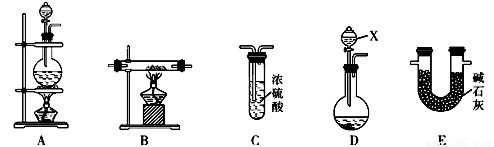
(1)某化学兴趣小组甲同学欲用加热NaNO2和NH4Cl的浓溶液制得N2,应该选择的发生装置是 ,在添加药品、制取气体前必须进行的操作是 。
(2)在加热条件下,用NH3还原CuO可制得N2,同时获得铜粉,此反应的化学反应方程式是 。
(3)乙同学利用②中反应原理制备干燥、纯净的N2,且需要的NH3以生石灰和浓氨水作原料。按气流从左到右的连接顺序是D→E→B→C,其中装置D中仪器X的名称是 。装置C中试剂的作用是 。
(1)A(2分);检查气密性(2分);
(2)3CuO+2NH3 N2+3Cu+3H2O(2分)
N2+3Cu+3H2O(2分)
(3)分液漏斗(2分);干燥N2并除去其中的NH3(2分)
【解析】
试题分析:(1)该反应中反应物是固体和液体、反应条件是加热,所以应该选取固液混合加热型装置,故选A;作有连接仪器的实验前要检查装置的气密性,该装置中需要连接仪器,所以作实验前要检查装置的气密性,否则易导致实验失败。
(2)该反应的反应物是NH3、CuO,生成物是N2、Cu,反应条件是加热,所以该反应方程式为:3CuO+2NH3 N2+3Cu+3H2O
N2+3Cu+3H2O
(3)根据装置图可知该仪器是分液漏斗;氨气属于碱性有刺激性气味的气体,不能直接排空,应该用酸吸收,则C装置的作用是干燥N2并除去其中的NH3。
考点:本题考查氮气的制取、基本仪器和基本操作、化学方程式的书写。


 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源:2015届浙江省温州市十校联合体高三上学期期初联考化学试卷(解析版) 题型:选择题
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
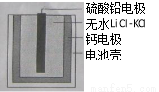
A.正极反应式:Ca+2Cl- - 2e- = CaCl2
B.常温时,在正负极间接上电流表或检流计,指针不偏转
C.放电过程中,Li+向负极移动
D.每转移0.1mol电子,理论上生成20.7g Pb
查看答案和解析>>
科目:高中化学 来源:2015届浙江省杭州地区六校高二下学期期中联考化学试卷(解析版) 题型:选择题
在日常生活和生产过程中化学有着重要的应用,下列有关说法正确的是
A.洪涝、地震灾区灾后常用石灰对环境进行消毒,是利用石灰可使蛋白质变性的性质
B.食品添加剂对人体均有益,因此在添加时无需对其用量进行严格控制
C.生活中常见的石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品
D.根据分散系的稳定性,将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中化学试卷(解析版) 题型:选择题
化合物丙(C4H8Br2)由如下反应得到: 则丙的结构不可能是
则丙的结构不可能是
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中化学试卷(解析版) 题型:选择题
已知化合物B3N3H6(硼氮苯)与C6H6(苯)的分子结构相似,如图。则硼氮苯的二氯取代物B3N3H4Cl2的同分异构体的数目为
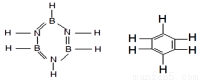
A.6 B.4 C.3 D.2
查看答案和解析>>
科目:高中化学 来源:2015届浙江省嘉兴市高二暑假作业检测(开学作业检测)化学试卷(解析版) 题型:选择题
下表为部分短周期元素化合价及其相应原子半径的数据。下列说法正确的是
元素性质 | 元素编号 | |||||||
A | B | C | D | E | F | G | H | |
原子半径(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
最高化合价 | +6 | +4 |
| +5 |
| +5 | +4 | +7 |
最低化合价 | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
A.C为硫元素
B.A、B是同周期元素
C.F、H的简单离子的电子层结构相同
D.元素G在周期中的位置是第二周期第Ⅳ族
查看答案和解析>>
科目:高中化学 来源:2015届浙江省嘉兴市高二暑假作业检测(开学作业检测)化学试卷(解析版) 题型:选择题
t℃时,10mL0.4mol?L?1H2O2溶液发生催化分【解析】
2H2O2=2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表
t/min | 0 | 2 | 4 | 6 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 |
下列叙述不正确的是(溶液体积变化忽略不计)
A.0~2min H2O2平及反应速率比4~6min快
B.0~6min的平均反应速率V(H2O2)≈3.3×10-2mol?L-1?min-1
C.反应至6min时,C(H2O2)=0.3mol?L?1
D.反应至6min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
按要求完成下列问题:
(1)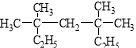 系统命名为 ;
系统命名为 ;
(2)4―甲基―1―戊烯的键线式为 。
(3)写出乙醛与新制氢氧化铜反应化学方程式 ;
(4)丙三醇与硝酸反应能生成三硝酸甘油酯,写出三硝酸甘油酯的结构简式
(5)下列有关实验的说法不正确的是_____________。
A.制乙烯时,温度计应插入反应混合液中
B.实验室用溴和苯在铁粉存在下反应,得到的溴苯显褐色,原因是溴苯在空气中被氧化
C.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液
D.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤
E.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少
查看答案和解析>>
科目:高中化学 来源:2015届浙江省“温州八校”高三返校联考化学试卷(解析版) 题型:选择题
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)
 CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2=ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com