
【题目】用下面两种方祛可以制得白色的Fe(OH)2沉淀。
方法一:用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)制取所需的FeSO4溶液需要的反应物为_______。
(2)生成白色Fe(OH)2沉淀的操作是用长滴管吸取NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。这样操作的理由是__________。
方法二:在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。

(3)在试管Ⅰ里加入的试剂是________________________________________。
(4)在试管Ⅱ里加入的试剂是________________________________________。
操作:先打开止水夹,使I管中反应一段时间后再夹紧止水夹,实验中观察到I管中溶液被压入II管中,II中发生反应的离子方程式为:_____________。
(5)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是_____________________。
【答案】稀H2SO4、铁屑避免生成的Fe(OH)2沉淀接触O2稀H2SO4、铁屑NaOH溶液Fe2++2OH-=Fe(OH)2↓试管I中反应生成的H2充满了试管I和试管II,且外界空气不容易进入
【解析】本题用两种方法来制备氢氧化亚铁,方法一完全是采用课本中的实验,考查硫酸亚铁的制备;在制备氢氧化亚铁时必须要除去溶解在溶液中的氧气.方法二是对课本实验的延伸,是一种改进的制备方法,用氢气作保护气的方法来保证新制的氢氧化亚铁不马上被氧化。
(1)铁与稀硫酸反应生成硫酸亚铁和氢气,所以制取所需的FeSO4溶液需要的反应物为稀H2SO4、铁屑;
(2)氢氧化亚铁很容易被空气中的氧气氧化,为了避免生成的Fe(OH)2沉淀接触O2,实验时生成白色氢氧化亚铁沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。
方法二(3)试管Ⅰ中提供还原性气体氢气和硫酸亚铁溶液,可用稀硫酸和铁屑反应生成,则在试管Ⅰ里加入的试剂是稀H2SO4、铁屑;
(4)试管Ⅱ中应为NaOH溶液,与试管Ⅰ中生成的FeSO4溶液反应生成Fe(OH)2沉淀。打开止水夹,Fe与H2SO4反应生成H2充满整个装置,反应一段时间后关闭止水夹,左侧试管内气压升高,反应生成的Fe2+沿导管进入右侧试管与NaOH反应生成白色沉淀氢氧化亚铁,所以II中发生反应的离子方程式为Fe2++2OH-=Fe(OH)2↓。
(5)试管I中反应生成的H2充满了试管I和试管II,且外界空气不容易进入,所以生成的Fe(OH)2沉淀能较长时间保持白色。


科目:高中化学 来源: 题型:
【题目】氯气的实验室制法是MnO2和浓盐酸在加热条件下反应,若将MnO2换成KMnO4、KClO3等氧化剂氧化浓盐酸亦可快速制取氯气。根据上述反应原理,有人提出猜想:能否利用Na2O2的强氧化性氧化浓盐酸得到氯气呢?某课外小组在实验室进行了探索性实验,设计了如图所示装置:

操作步骤及有关现象如下:
①装好装置,检查装置的气密性,加入药品。
②缓慢通入一定量的N2后,将装置E连接好(导管未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,反应剧烈,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体.装置E中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)用化学方程式表示实验室制取Cl2的反应:____________________________________;若以含14.6g HCl的浓盐酸与足量MnO2充分反应,制得的Cl2在标准状况下总小于2.24L,原因可能是____________________________________________________。
(2)装置B中为湿润的KI-淀粉试纸,反应一段时间后试纸变蓝,能否仅通过该现象说明A装置中产生氯气?___________(填“能”或“不能”),请用离子方程式说明原因________;装置C中湿润的红色布条褪色,是因为产生了具有强氧化性的物质:_____。
(3)实验证明,Na2O2可以与HCl反应生成氯气,请写出反应的化学方程式:_____________。
(4)装置D的作用之一是吸收生成的氯气,请写出相应的离子方程式:_________________。
(5)利用Na2O2与浓盐酸反应制得的Cl2中通常含有的杂质气体有:___________(不包括水蒸气),较难分离,因此实验室很少用该方法制取氯气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( ) 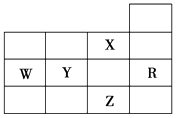
A.W元素的电负性大于Y元素的电负性
B.X元素是电负性最大的元素
C.p能级未成对电子最多的是Z元素
D.Y,Z的阴离子电子层结构都与R原子的相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( ) 
A.相对于途径②,途径①更好地体现了绿色化学思想
B.X可能是SO2和SO3的混合气体
C.Y可以是葡萄糖溶液
D.将CuSO4溶液蒸发,利用余热蒸干,可制得胆矾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用图中的装置可以实现该反应.回答下列问题:

(1)A中发生反应的化学方程式是_____.
(2)B中加入的物质是_____.
(3)实验时在C中观察到的现象是_____,发生反应的化学方程式是_____.
(4)实验时在D中收集到的物质是_____,检验该物质的方法和现象是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究铜及其化合物的性质对科研、生产生活有重要的意义.
(1)铜可采用如下方法制备
①火法炼铜:Cu2S+O2![]() 2Cu+SO2
2Cu+SO2
②湿法炼铜:CuSO4+Fe═FeSO4+Cu
上述两种方法中,铜元素均被 (填“氧化”或“还原”)成铜单质,若用①法每制得32gCu,转移电子的物质的量是 .
(2)在潮湿的空气中铜可以发生电化学腐蚀,生成铜绿,铜绿的化学式为 发生腐蚀的正极反应式为 ,由铜和锌组成的黄铜合金不易生锈,其防腐蚀的方法是 .
(3)①Li﹣﹣CuO电池总反应为:2Li+CuO═Li2O+Cu.电解质溶液为高氯酸锂有机溶液,电池的正极反应式为 .
②Cu2O是一种半导体材料,可在碱性溶液中用电解法制取,电解总反应式为:
2Cu+H2O![]() Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
Cu2O+H2↑,阳极反应式为 ;Cu2O投入稀硫酸中,得到蓝色溶液和红色沉淀,写出该反应的离子方程式 .
(4)为了回收粗铜精炼后阳极泥中的Ag和Au,某实验小组查阅了有关资料如下表:
编号 | 常温下反应 | 化学平衡常数 |
反应甲 | Au+6HNO3Au(NO3)3+3NO2↑+3H2O | <10﹣5 |
反应乙 | Au3++4Cl﹣[AuCl4]﹣ | >105 |
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为l:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第三代工业制取流程如图所示:
下列说法错误的是( )
A.Y、Z分别为H2、Cl2
B.制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1
C.SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价
D.Y与SiHCl3制备多晶硅的反应属于置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分 
(1)写出元素⑩的基态原子的电子排布简化式 , 外围电子排布图 . 指出它在周期表中的位置 . 焊接钢轨时,常利用⑩的某些氧化物与⑦的单质在高温下发生反应,试写出其中一条反应的化学方程式 .
(2)①③⑤三种元素可以形成多种有机化合物分子,其中最简单原子数最少的一种是室内装潢时形成的主要气体污染物.试写出它的电子式 , 推测该分子的空间构型为 .
(3)③④⑤⑥⑧五种元素都可以与元素①形成化合物,其中熔点最高的是(写化合物的化学式).如果在温度接近373K时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果总是比理论值高,其原因是 .
(4)某些不同族元素的性质也有一定的相似性,如图中元素⑦与元素②的氢氧化物有相似的性质.请写出元素②的氢氧化物与NaOH溶液反应的化学方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com