
【题目】某学习小组欲测定市售橙汁饮料中维生素C的含量。每100克鲜榨橙汁中含有大约37.5毫克的维生素C。实验室可用碘量法测定橙汁饮料中维生素C的含量,反应的方程式为C6H8O6+I2==C6H6O6+2HI(维生素C化学式为C6H8O6,相对分子质量为176),其实验步骤及相关数据如下:
①标准溶液的稀释:移取浓度为0.0080mol/L的碘标准溶液25.00mL于250mL容量瓶中,定容,摇匀备用。
②移取10.00mL饮料样品(设密度为1.0g/cm3)于250 mL锥形瓶中,加入50mL蒸馏水,2mL指示剂。
③在滴定管中装入稀释后的标准溶液,滴定至终点,读取并记录相关数据。
④重复测定3次,数据记录如下表。
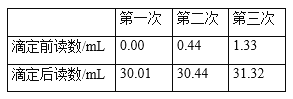
回答下列问题:
(1)实验中盛装标准溶液应选择______(填“酸式”或“碱式”)滴定管。
(2)步骤2中加入的指示剂是___________,判断滴定达到终点的现象是__________。
(3)实验中下列操作可能导致测定结果偏低的是_______(填标号)。
A.稀释标准溶液定容时俯视刻度线
B.滴定结束时俯视读
C.在锥形瓶中加入样品后放置较长时间才开始滴定
D.滴定管尖嘴部分有气泡,滴定后消失
(4)计算该饮料样品中维生素C含量为________mg/100 g。该含量______(填“高于”或“低于”)鲜榨橙汁。
【答案】酸式 淀粉溶液 溶液变为蓝色,且半分钟不褪色 ABC 42.2 高于
【解析】
⑴单质碘易腐蚀橡皮管。
⑵用单质碘滴定,得出加入的指示剂。
⑶A. 稀释标准溶液定容时俯视刻度线,溶液体积偏小,标液浓度偏大,所消耗标液体积减少,浓度偏低;B. 滴定结束时俯视读数,溶液体积偏小,测定结果偏低;C. 在锥形瓶中加入样品后放置较长时间才开始滴定,部分被被氧化,所消耗标液体积减少,测定结果偏低;D. 滴定管尖嘴部分有气泡,滴定后消失,得到消耗标液体积偏大,测定结果偏高。
⑷得出三次数据的平均值和碘标准溶液浓度,根据方程式得到10mL饮料中C6H8O6的物质的量,再得100g饮料样品中维生素C含量的质量。
⑴单质碘易腐蚀橡皮管,因此实验中盛装标准溶液应选择酸式滴定管;故答案为:酸式。
⑵用单质碘滴定,因此步骤2中加入的指示剂是淀粉溶液,判断滴定达到终点的现象是溶液变为蓝色,且半分钟不褪色;故答案为:溶液变为蓝色,且半分钟不褪色。
⑶A. 稀释标准溶液定容时俯视刻度线,溶液体积偏小,标液浓度偏大,所消耗标液体积减少,浓度偏低,故A符合题意;
B. 滴定结束时俯视读数,溶液体积偏小,测定结果偏低,故B符合题意;
C. 在锥形瓶中加入样品后放置较长时间才开始滴定,部分被被氧化,所消耗标液体积减少,测定结果偏低,故C符合题意;
D. 滴定管尖嘴部分有气泡,滴定后消失,得到消耗标液体积偏大,测定结果偏高,故D不符合题意。
综上所述,答案为ABC。
⑷三次数据的平均值为30.00mL,移取浓度为0.0080 molL1的碘标准溶液25.00 mL于250 mL容量瓶中,定容,摇匀备用,碘标准溶液浓度为0.0008 molL1,根据C6H8O6+I2 = C6H6O6+2HI得到10mL饮料即10g中C6H8O6的物质的量n(C6H8O6)= 0.0008 molL1×0.03L = 2.4×105 mol,则100g饮料样品中维生素C含量为2.4×105 mol ×10×176×103mg![]() mol1= 42.2mg,即该饮料样品中维生素C含量为42.2mg/100g该含量高于鲜榨橙汁;故答案为:42.2;高于。
mol1= 42.2mg,即该饮料样品中维生素C含量为42.2mg/100g该含量高于鲜榨橙汁;故答案为:42.2;高于。


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】常温下,向10 mL 0.1 mol/L的HR溶液中逐滴滴入0.l mol/L 的氨水,溶液pH及导电性变化如图。
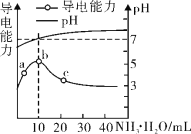
下列分析正确的是
A.HR为强酸
B.加入10 mL 氨水时,溶液中c(NH4+)>c(R-)
C.c点溶液存在c(NH4+)<c( R-)
D.b点的离子浓度大于a点的离子浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】PVAc是一种具有热塑性的树脂,可合成重要的高分子材料![]() ,合成路线如下:
,合成路线如下:
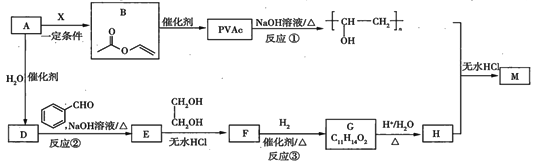
已知:
Ⅰ.![]() ;
;
Ⅱ.RCHO+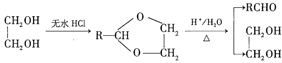
(1)标准状况下,![]() 气态烃
气态烃![]() 的质量是5.2g,则
的质量是5.2g,则![]() 的结构简式为___________。
的结构简式为___________。
(2)已知![]() 为加成反应,则
为加成反应,则![]() 的结构简式为_______;
的结构简式为_______;![]() 中所含官能团的名称是__________。
中所含官能团的名称是__________。
(3)反应①的化学方程式为__________________。
(4)反应③的化学方程式为__________________。
(5)在![]() 的转化过程中,乙二醇的作用是________________。
的转化过程中,乙二醇的作用是________________。
(6)已知![]() 的链节中除苯环外,还含有六元环状结构,则
的链节中除苯环外,还含有六元环状结构,则![]() 的结构简式为____________。
的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在试管中进行下列实验,现象与实验操作不相匹配的是
实验操作 | 实验现象 | |
A | 向硫酸铜水溶液中逐滴加入氨水 | 先产生蓝色沉淀,然后溶解,最后得到深蓝色透明溶液 |
B | 向I2的CCl4溶液中加入浓KI溶液,振荡 | 溶液紫红色变浅 |
C | 向橙色的K2Cr2O7溶液中加入10滴浓硫酸,振荡 | 溶液由橙色变为黄色 |
D | 向饱和硼酸溶液中加入Na2CO3溶液 | 无明显现象 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是重要的化工原料,利用合成气(CO、H2、CO2)在催化剂的作用下合成甲醇,可能发生的反应如下:
①CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH1=-49.58kJ/mol K1
CH3OH(g)+H2O(g) ΔH1=-49.58kJ/mol K1
②CO(g)+2H2(g)![]() CH3OH(g) ΔH2=-90.77 kJ/mol K2
CH3OH(g) ΔH2=-90.77 kJ/mol K2
③CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH3 K3
CO(g)+H2O(g) ΔH3 K3
(1)反应③的ΔH3=________,化学平衡常数K3与K1、K2的代数关系是K3=_____。
(2)要使反应②的速率和转化率都增大,需要改变的条件是___________。在5MPa下,要提高反应②的转化率,可采取的措施有__________、_________(答两条)。
(3)若反应①在恒容密闭容器中进行,下列可以判断该反应达到平衡的是_______(填标号)。
A.v正(H2)=v逆(CH3OH) B.混合气压强不变
C.c(H2)与c(H2O)比值不变 D.混合气密度不变
(4)在一定温度和催化剂存在下,向1L密闭容器中充入1molCO2和3molH2发生反应①。当CO2的平衡转化率为50%时,产物甲醇的体积分数为________,该温度下,正反应的平衡常数K=__________。若向容器中再充入0.5molH2和0.5molH2O(g),其他条件不变时平衡_______移动(填“正向”“逆向”“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的有机产物,肯定是一种的是( )
A. 异戊二烯(![]() )与等物质的量的Br2发生加成反应
)与等物质的量的Br2发生加成反应
B. 2—氯丁烷(![]() )与NaOH溶液共热发生反应
)与NaOH溶液共热发生反应
C. 甲苯在一定条件下发生硝化生成一硝基甲苯的反应
D. 等物质的量的甲烷和氯气的混和气体长时间光照后的产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家从腐败草中提取出一种能使血液不凝固的双豆香素M,M的结构简式如图所示。下列说法正确的是( )
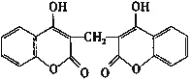
A.M能使溴水、酸性高锰酸钾溶液褪色,其褪色原理相同
B.M分子中所有原子可能处于同一平面
C.M分子中苯环上的一氯代物有4种
D.M分子有3种含氧官能团
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示。下列说法正确的是( )

A.m=2
B.在Xm-中,硼原子轨道的杂化类型相同
C.1、2原子间和4、5原子间的化学键可能是配位键
D.Xm-中含离子键和配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是( )
A.用来制造电线电缆的聚乙烯树脂属于热塑性高分子材料
B.研发可降解高分子材料,可以减少“白色污染”
C.棉、麻、羊毛及合成纤维完全燃烧都只生成![]() 和
和![]()
D.硅橡胶![]() 可由
可由![]() 经水解、缩聚两步反应制得
经水解、缩聚两步反应制得
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com