
已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
A.水的电离程度先减小再增大
B. 始终增大
始终增大
C.n (CH3COOH)与n (CH3COO-)之和始终保持不变
D.当加入氨水的体积为10 mL时,溶液的PH一定为7
C
【解析】试题分析:A. 醋酸电离:CH3COOH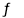 CH3COO-+H+,一水合氨电离:NH3H2O
CH3COO-+H+,一水合氨电离:NH3H2O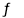 NH4++OH-,H2O的电离:H2O
NH4++OH-,H2O的电离:H2O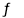 H++OH-,所以开始滴加氨水时,中和了醋酸电离出的H+使水的电离程度增大,当二者恰好完全反应后,再滴加氨水,会抑制水的电离,使其电离程度减小,A错误;B、因为NH3H2O的电离常数Kb= c(OH-)c(NH4+)/c(NH3H2O),所以c(NH4+)/c(NH3H2O)=Kb/c(OH-),因为Kb不变,c(OH-)逐渐增大,所以c(NH4+)/c(NH3H2O)始终减小,故B错误;C、根据原子守恒,n(CH3COOH)与n(CH3COO)之和是定值,故C正确;D、当加入氨水的体积为10mL时,CH3COOH和NH3H2O恰好完全反应,因为CH3COOH和NH3H2O 的电离常数相等, 则同浓度NH4+和CH3COO的水解程度相等,所以CH3COONH4呈中性,但由于不知温度,PH不能确定,故D错误。
H++OH-,所以开始滴加氨水时,中和了醋酸电离出的H+使水的电离程度增大,当二者恰好完全反应后,再滴加氨水,会抑制水的电离,使其电离程度减小,A错误;B、因为NH3H2O的电离常数Kb= c(OH-)c(NH4+)/c(NH3H2O),所以c(NH4+)/c(NH3H2O)=Kb/c(OH-),因为Kb不变,c(OH-)逐渐增大,所以c(NH4+)/c(NH3H2O)始终减小,故B错误;C、根据原子守恒,n(CH3COOH)与n(CH3COO)之和是定值,故C正确;D、当加入氨水的体积为10mL时,CH3COOH和NH3H2O恰好完全反应,因为CH3COOH和NH3H2O 的电离常数相等, 则同浓度NH4+和CH3COO的水解程度相等,所以CH3COONH4呈中性,但由于不知温度,PH不能确定,故D错误。
考点:了解水的电离,离子积常数。了解弱电解质在水中的电离平衡及影响因素和电离常数的意义。


科目:高中化学 来源:2014-2015福建省龙岩市非一级达标校高二上学期期末化学试卷(解析版) 题型:选择题
室温下,对于CH3COONa的说法下列判断正确的是
A.c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
B.升高温度,c(OH—)与c(CH3COO—)的比值将减小
C.CH3COONa稀溶液加水稀释时,溶液中各离子浓度均减小
D.c(CH3COO-)+ c(CH3COOH)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:实验题
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,下表是他们撰写的实验报告的一部分。
实验序号 | 实验步骤(内容) | 现象 |
① | 在贴有标签a、b的试管中分别加入1.0 g Na2CO3固体和NaHCO3固体,观察外观。 | |
② | 分别滴入几滴水,振荡,摸试管底部。 | 试管 放热现象更明显(填“a”或“b”)。 |
③ | 继续向两试管中分别加入10.0 mL水,用力振荡,观察现象。 | |
④ | 再分别向两试管中滴加2滴酚酞溶液,观察现象。 | 溶液均变红,颜色较深的试管是_________(填“a”或“b”)。 |
⑤ | 最后分别向两溶液中滴加足量盐酸。 | 红色褪去,均有无色气体产生。经计算生成气体的量a_____b(填“>”“<”或“=”)。 |
⑥ | 加热大试管一段时间。(注:棉花球沾有无水硫酸铜粉末)
|
(1)请帮助该小组同学完成实验报告中的内容。
(2)已知:20℃时Na2CO3的溶解度为20.5 g。由实验 (填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5 g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是 ,化学方程式是 。
(3)由实验⑥可以得出的结论是 ,用化学方程式说明得出结论的原因 。
查看答案和解析>>
科目:高中化学 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:选择题
向下列各物质的水溶液中滴加稀H2SO4或MgCl2溶液时,均有白色沉淀生成的是
A.BaCl2 B.Na2CO3 C.KOH D.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期第三次统练理综化学试卷(解析版) 题型:实验题
(16分)间硝基苯胺(Mr=128)是一种重要的染料中间体。它是一种黄色针状结晶,微溶于水,随温度升高溶解度增大,溶于乙醇、乙醚、甲醇。间硝基苯胺可选用间二硝基苯与碱金属多硫化物进行选择性还原,其反应式如下:

已知:R-NH2 + H+ → R-NH3+
实验步骤:
①在100mL锥形瓶中加入8g结晶硫化钠与30mL水,搅拌溶解。再加入2g硫黄粉,缓缓加热并不断搅拌到硫黄粉全部溶解,冷却后备用。
②在150mL三颈烧瓶中加入4.74g间二硝基苯(Mr=158)与40mL水,安装机械搅拌装置、滴液漏斗和回流冷凝管如图所示,将步骤①配制的多硫化钠溶液加入滴液漏斗。

③加热三颈烧瓶至瓶内微微沸腾,开动搅拌使间二硝基苯与水形成悬浮液。慢慢滴加多硫化钠溶液,滴加完毕后继续搅拌回流30min。移去热源,用冷水浴使反应物迅速冷却到室温后,减压过滤,滤饼洗涤三次。
④在150mL某容器中配制稀盐酸(30mL水加7mL浓盐酸),将上述粗产物转移进该容器,加热并用玻璃棒搅拌,使间硝基苯胺溶解,冷却到室温后减压过滤。
⑤冷却滤液,在搅拌下滴加过量浓氨水到pH=8,滤液中逐渐析出黄色的间硝基苯胺。
⑥冷却到室温后减压过滤,洗涤滤饼到中性,抽干,产物重结晶提纯,在红外灯下干燥,称重,得2.56g。
回答下列问题:
(1)滴液漏斗较普通分液漏斗的优点 ;第④步中配制稀盐酸的容器名称为 。
(2)间二硝基苯和间硝基苯胺都有毒,因此该实验应在 内进行。
(3)在铁和盐酸作用制得初生态氢原子(还原性远强于碱金属多硫化物)也可以将硝基还原为氨基,却未被采用,其可能原因为 。
(4)第④步用盐酸溶解粗产品,而不用水的原因 。
(5)第③步中滤饼洗涤三次,可选用的洗涤剂为( );第⑥步产物要进行重结晶,可选用的试剂为( )。
A.冷水 B.热水 C.乙醚 D.乙醇
(6)第③步中,搅拌使间二硝基苯与水形成悬浮液后再滴加多硫化钠溶液,其原因为 。
(7)第⑥步中要将滤饼洗涤到中性,检验方法为 。
(8)该反应的产率为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三上学期第三次统练理综化学试卷(解析版) 题型:选择题
化学与人类生活、能源开发、资源利用等密切相关。下列说法正确的是
A.塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用
B.硅燃烧放出的热量多,且燃烧产物对环境污染程度低,可做“未来石油”
C.用K2FeO4取代Cl2处理饮用水,可杀菌消毒,但不能沉降水中的悬浮物
D.研发使用高效催化剂,可提高反应中原料的转化率
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三上学期期中考试化学试卷(解析版) 题型:选择题
将质量为W1 g的钠、铝混合物投入一定量的水中充分反应,金属没有剩余,溶液澄清,共收集到标准状况下的气体V1 L。向溶液中逐滴加入浓度为a mol/L的盐酸,过程中有白色沉淀生成后又逐渐溶解,当沉淀恰好消失时所加盐酸体积为V2 L,将溶液在HCl气氛中小心蒸干得固体W2 g。下列所列关系式中正确的是
A.35.5a=(W2-W1)/V2 B.n(Al)> mol
mol
C.n(Na)+3n(Al)= mol D.aV2=
mol D.aV2=
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.以石墨为电极电解MgCl2溶液:2Cl—+2H2O Cl2+H2↑+2OH—
Cl2+H2↑+2OH—
B.强碱溶液中NaClO与Fe(OH)3反应:3ClO—+2Fe(OH)3=2FeO42—+3Cl—+H2O+4H+
C.Na2CO3溶液与少量AlCl3溶液反应:3CO32-+Al3++3H2O=3HCO3-+Al(OH)3↓
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2OH CH3COO-+NH4++3NH3+2Ag↓+H2O
CH3COO-+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三上学期期中考试化学试卷(解析版) 题型:填空题
(10分)某强酸性溶液X含有Ba2+、Al3+、NH 、Fe2+、Fe3+、CO
、Fe2+、Fe3+、CO 、SO
、SO 、SO
、SO 、Cl-、NO
、Cl-、NO 中的一种或几种,取该溶液进行实验,实验内容如下:
中的一种或几种,取该溶液进行实验,实验内容如下:

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是_____________________________________;
(2)写出有关离子方程式:
步骤①中生成A__________________;步骤②生成沉淀I__________________。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,而沉淀C物质的量0.07 mol,能说明该溶液不能确定的阴离子存在的理由是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com