
| A. |  | B. | 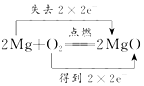 | ||
| C. | 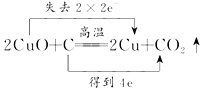 | D. | 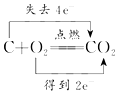 |
分析 A、反应中Cl元素化合价降低得电子,氧元素升高失电子,转移电子数为12;
B、Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4;
C、CuO与C反应,铜得电子,C失电子;
D、氧化还原反应中得失电子数应该相等.
解答 解:A、2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑中Cl元素化合价降低得电子,氧元素升高失电子,转移电子数为12,则电子转移的方向和数目为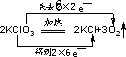 ,故A错误;
,故A错误;
B、Mg与氧气反应,Mg失电子,氧气得电子,转移电子数为4,则电子转移的方向和数目为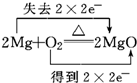 ,故B正确;
,故B正确;
C、CuO与C反应,铜得电子,C失电子,则电子转移的方向和数目为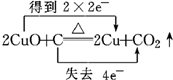 ,故C错误;
,故C错误;
D、氧化还原反应中得失电子数应该相等,则碳与氧气反应时,电子转移的方向和数目为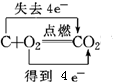 ,故D错误.
,故D错误.
故选B.
点评 本题考查氧化还原反应,侧重于学生的分析能力的考查,注意从元素化合价的角度分析,能用双线桥标出电子转移的方向和数目,难度不大.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:解答题
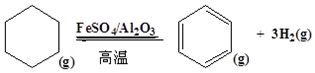
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ②③④ | C. | ①②④ | D. | ①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由水电离产生的c(H+)=1×10-12 mol•L-1的溶液中:K+、Na+、Fe2+、NO3- | |
| B. | 室温下,pH=7的溶液中:Al3+、Cl-、HCO3-、SO42- | |
| C. | 加酚酞呈红色的溶液中:CO32-、Cl-、F-、NH4+ | |
| D. | c(H+)/c(OH-)=1012的溶液中:NH4+、NO3-、Cl-、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL2mol/LMgCl2溶液 | B. | 1000mL2.5mol/LNaCl溶液 | ||
| C. | 300mL5mol/LFeCl3溶液 | D. | 250mL lmol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别加入足量锌片,两种溶液生成H2的体积相同 | |
| B. | 分别加水稀释100倍后,两种溶液的pH仍相同 | |
| C. | 醋酸中的c(CH3COO-)和硫酸中的c(SO${\;}_{4}^{2-}$)相等 | |
| D. | 两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
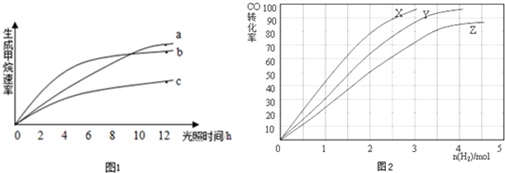
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com