
【题目】下列有关物质分类的说法中正确的是( )
A.树状分类法是唯一能表示物质分类的方法
B.在物质分类时,一般是先分类,再定标准
C.根据化合物在水溶液里或熔融状态下是否能导电,判断化合物是否为电解质
D.胶体、溶液、浊液的本质区别是其透过滤纸的性质不同
科目:高中化学 来源: 题型:
【题目】某研究性学习小组请你参与“铁及其化合物”有关性质的实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为_______________________________。
(2)反应前A中投放碎瓷片的目的是____________________。
(3)装置E中的现象是__________________________________。
探究二 FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I.实验需要90mL 0.10mol·L-1FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、玻璃棒、胶头滴管外还需的玻璃仪器是________。
(2)下列有关配制过程中说法正确的是________(填序号)。
a.用托盘天平称量质量为1.944g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90mL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II.探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1:Br-被Cl2氧化成Br2溶解在溶液中;
假设2:Fe2+被Cl2氧化成Fe3+。
(3)请你完成下表,验证假设
实验步骤、预期现象 | 结论 |
①向溶液中加入__________,振荡、静置, 现象:下层呈橙红色,上层呈无色 | 假设1正确 |
②向溶液中加入_____________ 现象:溶液变为红色 | 假设2正确 |
若假设1正确,从实验①中分离出Br2的实验操作名称是_______________ 。
(4)已知:Br2+2Fe2+=2Fe3++2Br-。若在50mL上述FeBr2溶液中通入标准状况112mlCl2,反应的离子方程式为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下图是中学化学常用的实验装置,诮回答下列问题

(1)用图I进行物质的分离提纯,该分离方法为________,若利用装置I分离酒精和水的混合物,还缺少的仪器__________;①的名称是__________,②的进水口是________(填“f" 或“g”)。
(2)现需配制500mL、0.1mol/LKCl 溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处: ①_________;②____________。
(3)仪器①~④中,使用时必须检查是否漏水的是_________(填序号)。
Ⅱ.分离和提纯物质的方法不仅用于实验研究而且广泛应用于工业生产和生活实际。
(4)海水晒盐过程中,通过蒸发的方法可得到粗盐固体;再将粗盐固体溶解后,再用过滤的方法除去其中的泥沙。粗盐中除泥沙外还含有可溶性杂质(如下表所示),可按下表所示由上至下的顺序依次除去(将表格填写完整)。
杂质 | 加入试剂的化学式 | 发生反应的离子方程式 |
硫酸盐 | ___________ | ___________ |
MgCl2 | NaOH | ___________ |
CaCl2 | Na2CO3 | ___________ |
依次加入上述试剂后,完全反应后,再进行过滤,再加入适量的盐酸 可除去上述步骤引入的 杂质离子。
(5) 从海带中可提取碘单质。用萃取的方法可将碘单质从水溶液中提取出来,该方法利用了I2在不同溶剂中的_______性不同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列鉴别Na2CO3和NaHCO3两种白色粉末的方案不能达到预期目的的是
A. 分别向等物质的量的白色粉末中加入足量盐酸,充分反应后,比较产生气体的体积
B. 分别向等物质的量的白色粉末中加入等体积、等浓度的稀盐酸,比较生成气体的快慢
C. 分别用图示装置进行实验,观察澄清石灰水是否变浑浊

D. 分别配成相同浓度溶液,滴加2滴酚酞试液后,比较溶液颜色的深浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图电解装置中,电极A是由金属M制成的,B、C和D都是铂电极,甲中的电解质溶液为MSO4 , 乙中的电解质为H2SO4 . E、F是外接直流电源的两极,电路接通后,电极B上有金属M析出.(已知金属M无变价) 
(1)电池中E是极,F是极.
(2)A极上电极反应为 , B极上电极反应为 , C极上电极反应为 , D极上电极反应为 .
(3)当电路中通过2.408×1022个电子时停止电解,发现B极上析出1.27gM,则金属M的相对原子质量为 .
(4)如果再将外接直流电源的正负极交换接入原电路,当通过1mol电子后,B极的电极反应为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.氧化还原反应中一定有化合价的升降
B.有氧元素参加的一定是氧化还原反应
C.氧化剂在反应中失去电子
D.还原剂在反应中化合价升高,被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列九种物质:①H2O,②Al,③CO2,④盐酸,⑤硫酸钡,⑥NaOH⑦饱和FeCl3溶液,⑧氨水,⑨乙醇。根据上述提供的物质,回答下列问题:
(1)属于电解质的是 _______________________(填序号),属于非电解质__________(填序号)。
(2)上述物质间发生的某反应的离子方程式为H++OH===H2O,则该反应的化学方程式为_________________________________________________________________________。
(3)实验室制备少量Fe(OH)3胶体所用的物质有__________(填序号),反应的离子方程式为____________________________________________________________________________。
(4)Al和Na的单质同时加入到一定量的水中,充分反应后,发现既无沉淀生成又无固体残留物存在,请用两个离子方程式表示其变化:______________________________; ____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃与苯在一定条件下反应生成芳香烃,如: ![]() +H2C=CH2
+H2C=CH2 ![]()
![]()
![]() +2H2C=CH2
+2H2C=CH2 ![]()
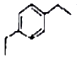
![]() +2H2C=CH2
+2H2C=CH2 ![]()
![]()
丙烯是三大合成材料的基本原料,可用于合成应用广泛的DAP树脂单体和双酚等有机物,具有重要的工业用途.
(1)写出丙烯在一定条件下发生聚合反应的化学方程式 .
(2)丙烯与苯在一定条件下反应可生成M、N等多种芳香烃.红外光谱、核磁共振是研究机物结构的重要方法,根据下列数据,写出M,N的结构简式. M:元素组成:C89.99%、H 10.06%;1H核磁共振有5个信号.
N:元素组成:C88.82%、H11.18%;1H核磁共振有3个信号.
M: , N: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com