
【题目】下列热化学方程式或离子方程式中,正确的是:
A. 甲烷的标准燃烧热为890.3kJ.mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ.mol-1
B. CO(g)的燃烧热是283.0 kJ/mol ,则CO2(g)=2CO(g)+O2(g)的反应热△H=+2×283.0 kJ/mol
C. NaOH和HCl反应的中和热 △H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol
D. 500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H=-38.6kJ/mol
2NH3(g) △H=-38.6kJ/mol
【答案】B
【解析】试题分析:A.甲烷的标准燃烧热为890.3kJmol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJmol-1,A错误;B.燃烧热是指25℃101KP时,1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,反应热与方程式的计量数成正比,CO(g)的燃烧热是283.0kJ/mol,则2CO(g)+O2(g)=2CO2(g)反应的△H=-2×283.0kJ/mol,B正确;C.中和热是指在稀溶液中,强酸和强碱反应生成1mol水时放出的热量,其衡量标准是生成的水为1mol,故无论稀H2SO4和Ca(OH)2反应生成的水是几摩尔,其中和热恒为57.3KJ/mol,C错误;D.相同条件下的同一可逆反应,正逆反应反应热数值相等,符号相反,0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,生成的氨气的物质的量小于1mol,所以2mol氨气分解,吸收的热量大于38.6kJ,D错误;答案选B。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、U、W 是原子序数依次增大的前四周期元素。其中 Y 的原子核外有 7 种运动状态不同的 电子;X、Z 中未成对电子数均为 2;U 是第三周期元素形成的简单离子中半径最小的元素;W 的内层电 子全充满,最外层只有 1 个电子。请回答下列问题:
(1)U 在周期表中的位置 。X、Y、Z 的第一电离能从大到小的顺序是 (用元素符号表示,下同)。
(2)写出 W 的价电子排布图 。
(3)根据等电子体原理,可知化合物 XZ 的电子式是 。
(4)X、Y、Z的最简单氢化物的键角从大到小的顺序是 ( 用化学式表示), 原因 是 。
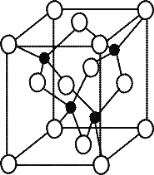
(5)由元素 Y 与 U 元素组成的化合物 A,晶胞结构如右图所示(黑球表示 Y 原子, 白球表示 U 原子),请写出化合物 A 的化学式 ,其中 Y 元素的杂化方式是 。
(6)U 的晶体属立方晶系,其晶胞边长为 405 pm,密度是 2.70 g/cm,通过计算确定 其晶胞的类型 (填简单立方堆积、体心立方堆积或面心立方最密堆 积)(已知:4053≈6.64×107)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铝、硅及其化合物在生产、生活中有广泛的用途。试回答下列问题:
(1)常用作红色油漆和涂料的铁的氧化物是__________(写化学式)。将少量该氧化物溶于稀盐酸中,并滴加几滴KSCN溶液,再加入过量的铁粉,振荡,这时看到的现象是_______________。
(2)“铝粉”的俗称为“银粉”,皆因铝粉色泽如银。“银粉”质轻,遇明火即炸,写出反应的化学方程式 _____________________。“银粉”与烧碱溶液反应的离子方程式为______________________。
(3)硅的原子结构示意图为____________,水玻璃可用作木材防火剂,其主要成分是(写化学式)________。写出工业生产粗硅的化学方程式_______________________。高温条件下,二氧化硅、碳粉、氮气以物质的量之比3∶6∶2反应可以生成氮化硅陶瓷(一种新型无机非金属材料,具有耐高温、耐磨、抗氧化等特性)和另一种气体化合物,该反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W的单质是空气中体积分数最大的气体,W与Y最外层电子数之和为X最外层电子数的2倍,X、Y、Z简单离子的电子层结构相同,Z最外层电子数等于最内层电子数。下列说法正确的是( )
A. 单质Z可用海水作原料获得
B. W的简单气态氢化物比Y的简单气态氢化物稳定
C. 原子半径由大到小的顺序:Z、Y、X、W
D. WX与ZX中的化学键类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
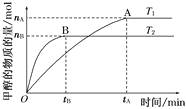
下列说法正确的是 (填序号)
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(2) 用乙醇燃料电池做电源进行工作,KOH溶液做电解质,写出负极的电极反应式为:____________。电池工作一段时间后溶液PH值___________(变大,变小或不变)
(3) 若在常温常压下,1克乙醇完全燃烧生成二氧化碳和液态水放热约为30KJ的热量,写出乙醇燃烧热的热化学方程式________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。已知:酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易水解,易被氧化。某研究小组设计SnSO4制备路线如下:
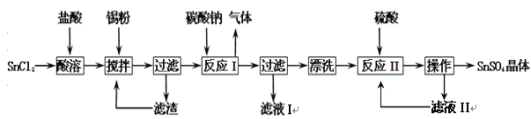
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是 ;
(2)反应I得到的沉淀是SnO,得到该沉淀的离子方程式是 ;
(3)在反应I得到沉淀SnO后,要进行“过滤”、“漂洗”,检验SnO是否洗涤干净的操作是 ;
(4)反应II之后的“操作”依次为 、 、过滤、洗涤、低温干燥;
(5)某化学兴趣小组对用于微电子器件生产的锡粉进行了纯度测定:①取1.19 g试样溶于稀硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;②加入过量的Fe2(SO4)3溶液;③用0.2000 mol/L 酸性K2Cr2O7溶液滴定(产物中Cr呈+3价)至终点,消耗K2Cr2O7溶液15.00 mL。写出酸性K2Cr2O7溶液滴定的离子方程式 ,则此锡粉样品中锡的质量分数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定密闭容器中发生反应H2(g)+I2(g) ![]() 2HI(g), 下列说法能说明此反应已经达到平衡状态的是
2HI(g), 下列说法能说明此反应已经达到平衡状态的是
A.容器内每减少1mol I2,同时生产2mol HI
B.容器内气体压强不再变化
C.混合气体的颜色不再变化
D.混合气体的密度恒定不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com