
【题目】在![]() 某一元碱(
某一元碱(![]() )中,滴加入
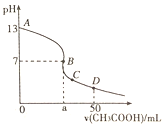
)中,滴加入![]() 的醋酸溶液,滴定曲线如图所示。下列说法错误的是( )
的醋酸溶液,滴定曲线如图所示。下列说法错误的是( )
A.该碱溶液可以溶解![]()
B.![]() 点对应的体积大于
点对应的体积大于![]()
C.![]() 点时,
点时,![]()
D.![]() 点时,
点时,![]()
【答案】D
【解析】
A. 由A点知:0.1molL1一元碱的pH=13可得,该碱为强碱,所以该碱溶液可以溶解![]() ,故A正确;
,故A正确;
B. 恰好中和时生成强碱弱酸盐pH应大于7,而B点pH=7,所以该点对应的溶质为CH3COOY和CH3COOH,a点的体积大于25mL,故B正确;
C. C点对应的溶质为CH3COOY和CH3COOH,溶液中CH3COOY的浓度>CH3COOH的浓度,因pH<7,所以c(H+)>c(OH),弱酸的电离是微弱的,结合电荷守恒c(CH3COO)+c(OH)=c(H+)+c(Y+),则应有c(CH3COO)>c(Y+)> c(H+)>c(OH),故C正确;
D. D点为CH3COOY和CH3COOH等物质的量浓度的混合液,根据物料守恒c(CH3COO)+c(CH3COOH)=2c(Y+)和电荷守恒c(CH3COO)+c(OH)=c(H+)+c(Y+),所以应有![]() ,故D错误;
,故D错误;
答案选D。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
【题目】某班几个兴趣小组做了以下实验。
甲组:两同学利用下列试剂:铁粉、0.1mol/L FeCl3溶液、0.1mol/L FeCl2溶液、KSCN溶液、新制氯水,探究Fe2+、Fe3+ 的性质,设计实验方案进行实验,完成下列表格。
探究内容 | 实验方案 | 实验现象 | 写出离子方程式 |
①探究Fe2+具有还原性 | 取少FeCl2溶液,加入少量KSCN溶液后,再往溶液中加入少量________。 | 溶液先不变红,后变为血红色。 | Fe2+发生的反应: _____________ |
②探究Fe3+具有氧化性 | 取少量FeCl3溶液,加入足 量______后,振荡,静置,再往溶液中加入少量KSCN溶液。 | 溶液不变为血红色。 | Fe3+发生的反应:________ |
乙组:两同学利用下图所示的装置进行铁与水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
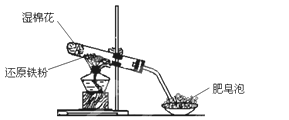
请回答下列问题。
(1)硬质试管中发生反应的化学方程式为_______________。
(2)欲确定反应后硬质试管中固体物质的成分,实验过程如下:
①待硬质试管冷却后,取少许其中的固体物质溶于足量稀硫酸得溶液B;
②取少量溶液B于试管a中,滴加KSCN溶液,溶液没有变红色,则溶液B中的阳离子有_________________,硬质试管中固体物质的成分是_________________。
(3)另取少量溶液B,使其与NaOH溶液反应(按图所示),在胶头滴管挤出NaOH溶液的瞬间可观察到生成白色沉淀,沉淀迅速变成灰绿色,最后变成红褐色。请写出与上述现象中白色沉淀转化红褐色沉淀的化学方程式________________。
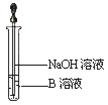
(4)一段时间后,发现a中未变红的溶液变成红色,原因是 _______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从甜橙的芳香油中可分离得到如图结构的化合物,
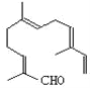
现有试剂:①KMnO4酸性溶液;②H2/Ni;③Ag(NH3)2OH;④新制Cu(OH)2,能与该化合物中所有官能团都发生反应的试剂有( )
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学欲除去固体氯化钠中混有的氯化钙,请据如下实验方案回答问题。
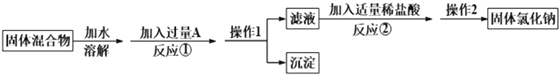
(1)操作1的名称是_____;
(2)反应①中加入略过量的A物质的目的是__________;
(3)写出反应②的化学方程式:_______。
(4)实验时称取样品的质量为185.0g,经过操作1后,测得沉淀(不溶于水)的质量为50.0g, 则样品中NaCl的质量分数是多少___?(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,属于烃的衍生物的是
①CH4 ②CH2=CH2 ③CH ![]() CH ④CH3CH2OH ⑤CH3CHO、⑥CH3COOH ⑦CH3COOCH2CH3⑧CH3CH2Cl
CH ④CH3CH2OH ⑤CH3CHO、⑥CH3COOH ⑦CH3COOCH2CH3⑧CH3CH2Cl
A.①②④⑤⑥B.②③④⑤⑥C.④⑤⑥⑦⑧D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年11月《Nature Energy》报道了巾科院大连化学物理研究所科学家用Ni- BaH2 /Al2O3、Ni- LiH等作催化剂,实现了在常压、100-300℃的条件下合成氨。
(1)在元素周期表中,氧和与其相邻且同周期的两种元素的第一电离能由大到小的顺序为 __ ;基态Ni2+的核外电子排布式为 ___,若该离子核外电子空间运动状态有15种,则该离子处于 ___(填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中NO3的空间构型为____。
②甘氨酸中N原子的杂化类型为____,分子中σ键与π键的个数比为____,晶体类型是 ___,其熔点、沸点远高于相对分子质量几乎相等的丙酸(熔点为-2l℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是____。
(3)NH3分子中的键角为107°,但在[Cu(NH3)4]2+离子中NH3分子的键角如图l所示,导致这种变化的原因是____
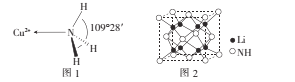
(4)亚氨基锂(Li2NH)是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图2所示,若晶胞参数为d pm,密度为ρg/cm3,则阿伏加德罗常数NA=____(列出表达式)mol-l。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为烃的衍生物,它们之间的转化关系如图所示,A俗称酒精;C的分子式为C2H4O2。完成下列填空:
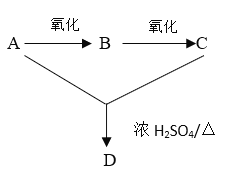
(1)写出由A转化为B的化学方程式_______________。检验B的试剂为 ________________。
(2)C中的官能团是_______________。
(3)D的结构简式为_______________;D与CH3CH2CH2COOH互为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
A.Na2O2+2HCl=2NaCl+H2O2
B.Ag2O+H2O2=2Ag+O2+H2O
C.2H2O2=2H2O+O2
D.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)H2O2仅体现氧化性的反应是(填代号) 。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号) 。
(3)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO![]() +5e-+8H+===Mn2++4H2O
+5e-+8H+===Mn2++4H2O
写出该氧化还原反应的化学方程式:_______________________。
(4)请配平以下化学方程式:
![]() Al+
Al+![]() NaNO3+
NaNO3+![]() NaOH===
NaOH===![]() NaAlO2+
NaAlO2+![]() N2↑+
N2↑+![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象,推出的相应结论正确的是
实验 | 现象 | 结论 |
A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
B.向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C.将足量SO2气体通入石蕊试液中 | 石蕊试液变红色 | SO2水溶液显酸性 |
D.向酸性KMnO4溶液中通入SO2 | 溶液紫色褪去 | SO2具有漂白性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com