
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,常温下是一种橙黄色有恶臭的液体,它的分子结构如图所示.

(1)S2Cl2的结构式为 ,其化学键类型有 (填“极性键”“非极性键”或“极性键和非极性键”).
(2)电负性:S (填“>”或“<”)Cl,S2Cl2中硫的化合价为 .
(3)S2Cl2分子中S原子的杂化轨道类型为 ,每个S原子有 对弧电子对.
【答案】(1)Cl﹣S﹣S﹣Cl;极性键和非极性键;
(2):<;+1;
(3)sp3;2.
【解析】
试题分析:(1)根据S2Cl2的结构式可知,其结构式为Cl﹣S﹣S﹣Cl,含有极性键Cl﹣S和非极性键S﹣S键;
(2)元素吸电子能力越强,非金属性越强,其电负性越强;由于电负性氯大于硫,故氯显﹣1价,S为+1价;
(3)价层电子对数=σ键个数+孤电子对数,根据价层电子对数确定其杂化类型和孤对电子对数.
解:(1)根据S2Cl2的结构式可知,其结构式为Cl﹣S﹣S﹣Cl,含有极性键Cl﹣S和非极性键S﹣S键,故答案为:Cl﹣S﹣S﹣Cl;极性键和非极性键;
(2)元素吸电子能力越强,非金属性越强,其电负性越强,非金属性S<Cl,电负性S<Cl;由于电负性氯大于硫,氯显﹣1价,S为+1价,故答案为:<;+1;
(3)价层电子对数=σ键个数+孤电子对数,S2Cl2分子中每个S原子价层电子对数=2+2=4,所以采取sp3杂化,含有2对孤对电子对,故答案为:sp3;2.


科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素主要化合价与原子序数的关系图,下列说法不正确的是( )
A. X和W位于同一主族
B. 原子半径:Y>Z>X
C. 盐YRX与化合物WX2的漂白原理相同
D. Y和R两者的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国稀土资源丰富。下列有关稀土元素![]() 与
与![]() 的说法正确的是( )
的说法正确的是( )
A. ![]() 与
与![]() 互为同位素
互为同位素
B. ![]() 与
与![]() 的质量数相同
的质量数相同
C. ![]() 与
与![]() 是同一种核素
是同一种核素
D. ![]() 与
与![]() 的核外电子数和中子数均为62
的核外电子数和中子数均为62
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol葡萄糖能水解生成2 mol CH3CH2OH和2 mol CO2
B.在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀
C.油脂不是高分子化合物,1 mol油脂完全水解生成1 mol甘油和3 mol高级脂肪酸
D.欲检验蔗糖水解产物是否具有还原性,可向水解后的溶液中直接加入新制的Cu(OH)2悬浊液并加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2一二氯乙烯有如图两种结构
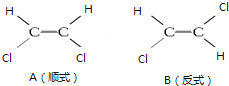
试回答下列问题:
(1)A、B分子中所含化学键类型__________(填“相同”或“不同”,下同),分子极性___________;
(2)A、B两种分子在CCl4中溶解度较大的是_________________;
(3)将A、B加入Br2的CCl4溶液中,可得物质C,则C的结构简式为__________,C物质_________(填“有”或“无”)手性异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某气体的分子为双原子分子,其摩尔质量为M gmol﹣1,现有标准状况下V L该气体,设阿伏加德罗常数的值为NA,则:
①该气体的物质的量为 mol;
②该气体中所含的原子总数为 ;
③该气体在标准状况下的密度为 gL﹣1;
④该气体的一个分子的质量为 g.
(2)气体化合物A分子式可表示为OxFy,已知同温同压下10mL A受热分解生成15mL O2和10mL F2,则A的化学式为 ,推断的依据为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的分子式为C10H14,它不能使溴水褪色,但能使酸性KMnO4溶液褪色,分子结构中只含有一个烷基。符合上述条件的烃有( )
A.2种 B.3种
C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法有不同的冶炼方法。火法炼铜:将辉铜矿(Cu2S)在空气中高温焙烧即可得到铜和一种还原性的气体。近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐。某工厂运用该原理生产铜和绿矾(FeSO47H2O)的工艺如下:
回答下列问题:
(1)火法炼铜发生的化学方程式:_________________________;
(2)湿发炼铜工艺流程中,为了提高酸浸时的进取率,本流程可采取的措施是________,试剂X为__________,其作用是_____________。
(3)试剂a为______________,试剂b为______________;
(4)配平反应1的化学方程式:____CuFeS2+___H2SO4+____O2=____CuSO4+____Fe2(SO4)3+____H2O
(5)已知:常温下Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.6×10-39。加入过量的试剂X调节pH=4时,可使溶液中的Fe3+转化为Fe(OH)3沉淀,则溶液中的c(Fe3+)=___________。若要此时不出现Cu(OH)2沉淀,则溶液中的Cu2+浓度最大不超过_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列有关说法不正确的是 ( )
A.淀粉、蛋白质、脂肪都属于营养物质
B.误食重金属盐,可立即喝牛奶或生蛋清进行解毒
C.新居室内装饰材料中缓慢释放出的甲醛等有机物会污染室内空气
D.棉线和毛线的主要成分都是纤维素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com