
【题目】下列物质在水溶液中关于电离方程式错误的是
A. MgCl2 = Mg2+ + 2Cl
B. Ba(OH)2 = Ba2+ + 2OH
C. CH3COOH = H+ + CH3COO-
D. KHSO4 = K+ + H+ + SO42-
【答案】C
【解析】
氯化镁为强电解质,完全电离生成镁离子和氯离子;氢氧化钡是强电解质,完全电离生成钡离子和氢氧根离子;醋酸是弱电解质,部分电离,用可逆号连接;HSO4-为强酸的酸式酸根离子,拆分为氢离子和硫酸根离子。
氯化镁为强电解质,完全电离,电离方程式为:MgCl2═Mg2++2Cl-,故A正确;氢氧化钡是强电解质,完全电离,电离方程式为:Ba(OH)2═Ba2++2OH-,故B正确;醋酸是弱电解质,部分电离,电离方程式是CH3COOH![]() H+ + CH3COO-,故C错误;HSO4-为强酸的酸式酸根离子,KHSO4在溶液中的电离方程式是KHSO4 = K+ + H+ + SO42-,故D正确。
H+ + CH3COO-,故C错误;HSO4-为强酸的酸式酸根离子,KHSO4在溶液中的电离方程式是KHSO4 = K+ + H+ + SO42-,故D正确。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 把100 mL3mol/LH2SO4跟100 mL H2O混合后,溶液中c(H+)为1.5 mol/L
B. 把100 mL 20% NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10%
C. 把200 mL3 mol/LBaCl2溶液跟100 mL3mol/LKCl溶液混合后,溶液中c(Cl-)仍然是3mol/L
D. 把100 g 20% NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,甲同学设计了如下图所示的实验装置,按要求回答问题。(提示:无水硫酸铜遇水变蓝;氯气易溶于CCl4等有机溶剂)
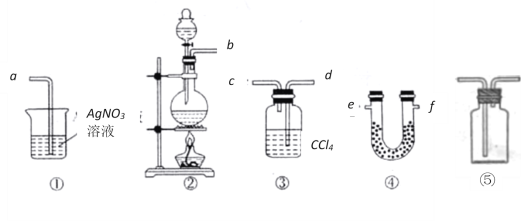
(1)根据甲同学的意图,连接相应的装置,接口顺序为:b接___,____接_____,____接a。
(2)在连接好装置之后实验开始之前必须要进行的一项操作是:___________________。
(3)U形管中所盛试剂的化学式为___________;装置③中CCl4的作用是____________。
(4)乙同学认为甲同学实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之
间再加装置⑤,你认为装置⑤应加在__________________之间(填装置序号),瓶中可以放入_________________________________。
(5)若在装置完好的前提下,用浓度为10mol/L的浓盐酸600mL与过量的的MnO2反应,最终生成的氯气_____1.5mol(填大于、小于或等于),其主要原因是___________________________,可以通过向反应后的溶液中加入___________来证明上述结论。
A.锌粒 B.氢氧化钠溶液 C.硝酸酸化的硝酸银溶液 D.碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.10 mol/L甲胺的溶液中滴加0.10 mol/L盐酸时混合溶液的pH与相关微粒的浓度关系如图所示。已知:甲胺(CH3NH2)类似于氨,但碱性稍强于氨。下列说法不正确的是

A. 甲胺在水中的电离方程式CH3NH2+H2O![]() CH3NH3++OH—
CH3NH3++OH—
B. b点对应的加入盐酸的体积小于20mL
C. 将等物质的量的CH3NH2和CH3NH3Cl一起溶于蒸馏水,得到对应a点的溶液
D. 常温下,甲胺的电离常数为Kb,则pKb=—lgKb=3.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误是的( )
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中含有的共价键一定非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于烷烃的叙述中,不正确的是( )
A. 甲烷是最简单的烷烃,是沼气、天然气的主要成分
B. 在烷烃分子中,所有的化学键都是单键
C. 分子通式为CnH2n+2的烃不一定是烷烃
D. 烷烃不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】浓硫酸与下列物质作用时,既表现氧化性,又表现酸性的是( )
①炽热的木炭 ②H2S气体 ③Cu(加热条件下) ④FeO ⑤NH3 ⑥蔗糖 ⑦CuSO4·5H2O ⑧铁、铝(常温下)
A.③④B.①②⑤⑧C.①②③④⑦D.⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组为了探究原电池反应,做了如下实验:将Al片和Zn片插入到Na2SO4溶液中,装置如下图。
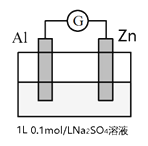
操作 | 现象 |
i接通电流计 | 接通开始之后指针向右偏且稳定;两极附近均没有明显现象。 |
ii向溶液中加入50mL 2mol/L H2SO4 | 开始时指针仍向右偏,Al、Zn表面均产生少量气泡;大约半分钟后,指针向左偏且稳定,Al、Zn表面均产生大量气泡。 |
下列说法不正确的是
A. i中指针向右偏时,Al的电极反应为:O2 + 4e- +2H2O = 4OH-
B. ii中开始时, Zn做负极,SO42-向Zn极移动
C. ii中半分钟后,装置中的反应为Al的析氢腐蚀和Al的化学腐蚀共存
D. 从上述实验中可以得出,Al在H2SO4中的还原性强于在Na2SO4中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com