
��X��Y��Z��W��M���ֶ�����Ԫ�أ�����X��Y��Z��Wͬ���ڣ� Z��Mͬ���壻 X+��M2-������ͬ�ĵ��Ӳ�ṹ�����Ӱ뾶��Z2-��W-��Y�ĵ��ʾ����۵�ߡ�Ӳ�ȴ���һ����Ҫ�İ뵼����ϡ�����˵���У���ȷ����( )
A. Ԫ��W��M��ij�ֵ��ʿ���Ϊˮ�����е������� B.��Ԫ��M��Zֻ���γ�һ�ֻ�����
C.Ԫ��Y��Z��W�ĵ��ʾ�������ͬ�����͵ľ��� D. X��M����Ԫ��ֻ���γ�X2M�ͻ�����
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʾ��ͼ���Ӧ�ķ�Ӧ�����ȷ����
A����0.01 mol KOH��0.01 mol Ca(OH)2�Ļ����Һ�л���ͨ��CO2
B��NaHSO4��Һ����μ���Ba(OH)2��Һ
C��KAl(SO4)2��Һ����μ���Ba(OH)2��Һ
D�����������������Ƶ�ƫ��������Һ�еμ�����
A B C D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1L1mol��L-1NaOH��Һ����0.6molCO2��������Һ��Na2CO3��NaHCO3�����ʵ���֮��ԼΪ�� ��
A��2�U3 B��1�U2 C��2�U1 D��3�U2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ǰ������Ԫ�صĻ�̬ԭ���У�δ�ɶԵ���������������������ͬ��Ԫ���У� ��
A��3�� B��4�� C��5�� D��6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����(�� ��)
A�����ۺ���ά��ˮ�����ղ��ﶼ�������� B����֬ˮ��ɵõ����������
C��������ˮ������ղ����Ƕ��� D��ʯ�͵ķ����ú�ĸ������˻�ѧ�仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ҫ�İ뵼����ϣ��������ִ����ӹ�ҵ�Ļ������ش���������:
(1)��̬Siԭ���У�����ռ�ݵ�������ߵĵ��Ӳ�ķ���Ϊ ���õ��Ӳ���е�ԭ�ӹ����Ϊ ��
(2)����Ҫ�Թ����Ρ� �Ȼ��������ʽ�����ڵؿ��С�
(3)���ʹ��������ʯ�ṹ���Ƶľ��壬����ԭ����ԭ��֮���� ���ϣ��侧��ƽ��ӵ��8����ԭ�ӣ�����������λ�ù��� ��ԭ�ӡ�
(4)���ʹ��ͨ������(SiH4)�ֽⷴӦ���Ʊ�����ҵ�ϲ���Mg2Si��NH4Cl��Һ�������з�Ӧ�Ƶ�SiH4��ͬʱ����һ�ֿ�ʹʪ��ĺ�ɫʯ����ֽ���������壬�÷�Ӧ�Ļ�ѧ����ʽΪ ��
(5)̼����йػ�ѧ������������ʾ����Ҫ�����ͽ��������й���ʵ��

�ٹ���̼ͬ�壬Ҳ��ϵ���⻯�������������������϶�Զ���������࣬ԭ���� ��
��SiH4���ȶ���С��CH4���������������ԭ���� ��
(6)�ڹ������У�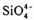 ������(����ͼ(a))ͨ�����ö��������ӿ��γɵ�״����״����״���Ǽ���״�Ĵ���ṹ��ʽ��ͼ(b)Ϊһ�����������ṹ�Ķ�����������Si��O��ԭ����֮��Ϊ ��ѧʽΪ ��
������(����ͼ(a))ͨ�����ö��������ӿ��γɵ�״����״����״���Ǽ���״�Ĵ���ṹ��ʽ��ͼ(b)Ϊһ�����������ṹ�Ķ�����������Si��O��ԭ����֮��Ϊ ��ѧʽΪ ��
 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ʷ����У�ǰ�߰������ߵ���
A�������� B������ʡ�������
C����Һ�� ���� D�����Ϸ�Ӧ�� �ӳɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����֮Ϊ������ء���ֽ�ʵ�أ�����һ������ֽƬ��Ϊ�����壬����һ�߶�п����������һ�߶ƶ������̡���ֽ�ڵ����ӡ�������ˮ������п��ɵĵ��Һ������ܷ�ӦΪ��
Zn + 2 MnO2 + H2O == ZnO + 2MnO (OH) ������˵����ȷ����
A���õ�ص�����Ϊп
B���õ�ط�Ӧ�ж����������������
C���� 0.l mol Zn ��ȫ��Ӧʱ���������Һ�ĵ��Ӹ���Ϊ 1.204��l023
D�����������ӦʽΪ�� 2MnO2 + 2H2O + 2e - ==2MnO (OH) + 2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������һ������O4���й�����������˵����ȷ����
A.���Ľṹ��P4��ͬ B.����Ħ������Ϊ64
C.����������ͬ�������� D.����������������ͨ�����Ӽ���������϶��ɵ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com