
��Ҫ��������и�С�⡣
��CO��H2�Ļ�������׳ƺϳ�������һ����Ҫ�Ĺ�ҵԭ��������̿����Ȼ������Ҫ�ɷ�ΪCH4�������͡�ú�ڸ����¾�����ˮ������Ӧ�Ƶúϳ�����
��1����֪ij��Ӧ��ƽ�ⳣ������ʽΪ��
������Ӧ�Ļ�ѧ����ʽΪ�� ��
��2�������Ϊ2L���ܱ������г���CH4��H2O(g)��ɵĻ��������1mol������һ�������·�����Ӧ�����ﵽƽ��״̬������¶ȡ�ѹǿ��Ͷ�ϱ�X��n(CH4)/n(H2O)���Ը÷�Ӧ��Ӱ����ͼ��ʾ��

��ͼ1�е�����������ʾͶ�ϱȵĹ�ϵX2 ____ X1(�=����>����<����ͬ)
��ͼ2������������ʾ��ѹǿ�ȵĹ�ϵ��P2 _______P1
��3����CH4��O2Ϊԭ�Ͽ���Ƴ�ȼ�ϵ�أ�
����װ����ʢ��150.0mL 1.0mol/L KOH��Һ���ŵ�ʱ���뷴Ӧ�������ڱ�״���µ����Ϊ4.48L������ŵ������û�������ݳ�����ŵ���Ϻ�������Һ�и�����Ũ���ɴ�С�Ĺ�ϵΪ��
����H2SO4��Һ����KOH��ҺΪ�������Һ,��CH4��ΪC6H12O6 ����ȼ�ϵ�صĸ�����ӦʽΪ��
��
��1��ij�¶�(t��)ʱ�����0.01mol��L-1��NaOH��Һ��pH��11���ڴ��¶��£���pH��2��H2SO4��ҺVaL��pH��12��NaOH��ҺVbL��ϣ������û��ҺΪ���ԣ���Va�UVb�� ��
(2)��25��ʱ����c mol��L-1�Ĵ�����Һ��0.02 mol��L-1NaOH��Һ�������Ϻ���Һ�պó����ԣ��ú�c�Ĵ���ʽ��ʾCH3COOH�ĵ��볣��Ka=____________________��
��14�֚���2�֣�
��1�� C��S��+H2O(g) H2(g) + CO(g) ���ɲ���״̬����д�����0�֣�
H2(g) + CO(g) ���ɲ���״̬����д�����0�֣�
��2�� �٣� ���ڣ�
��3����c(K+)��c(HCO3-)��cCO32-)��c(OH-)��c(H+)����C6H12O6��24e-+6H2O��6CO2��24H+
��1��10�U1 ��2��2��10-9/��c��0.02��
��������
�����������1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը���ƽ�ⳣ���ı���ʽ��֪���÷�Ӧ�Ļ�ѧ����ʽ��C��S����H2O(g) H2(g)��CO(g)��
H2(g)��CO(g)��
��2���ٸ��ݷ�Ӧ�Ļ�ѧ����ʽCH4��H2O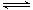 CO��3H2��֪�����¶���ͬʱ��Ͷ�ϱ�Խ�����ת����Խ�ͣ��������м���ĺ���Խ�ߣ����Ը���ͼ��1��֪��X2��X1��
CO��3H2��֪�����¶���ͬʱ��Ͷ�ϱ�Խ�����ת����Խ�ͣ��������м���ĺ���Խ�ߣ����Ը���ͼ��1��֪��X2��X1��
�ڸ��ݷ���ʽ��֪���÷�Ӧ���������ģ�������Ͷ�ϱ���ͬ�������£�ѹǿԽ�����ת����ԽС�������ĺ���Խ�ߣ����Ը���ͼ 2��֪��P2��P1��
��3�����ڸ�ȼ�ϵ���У������ڸ���ͨ�룬����������ͨ�롣�μӷ�Ӧ��������0.2mol���õ�0.8mol���ӣ��������ļ�������ʵ�����0.8mol��8��0.1mol������CO2��0.1mol������Һ������������0.15mol�����Է�Ӧ������̼��غ�̼����أ��Ҷ��ߵ����ʵ�������0.05mol������CO32����ˮ��̶ȴ���HCO3����ˮ��̶ȣ����Էŵ��������Һ�и�����Ũ���ɴ�С�Ĺ�ϵΪc(K+)��c(HCO3-)��cCO32-)��c(OH-)��c(H+)��
��ԭ����и���ʧȥ���ӣ������������ڸ����ŵ磬�缫��Ӧʽ��C6H12O6��24e-+6H2O��6CO2��24H+��
��1��ij�¶�(t��)ʱ�����0.01mol��L-1��NaOH��Һ��pH��11�����Ը��¶���ˮ�����ӻ�������1��10��13������pH��12��NaOH��Һ��OH����Ũ����0.1mol/L�����û��ҺΪ���ԣ���˵������ǡ�÷�Ӧ����VaL��0.01mol/L��VbL��0.1mol/L�����Va�UVb��10�U1��
��2����25��ʱ����c mol��L-1�Ĵ�����Һ��0.02 mol��L-1NaOH��Һ�������Ϻ���Һ�պó����ԣ���˸��ݵ���غ��֪����Һ��c(CH3COO��)��c(Na��)��0.01mol/L������Һ��c(CH3COOH)����0.5c��0.01��mol/L������Ϊ��Һ��c(H��)��1��10��7mol/L�����Ը��ݴ���ĵ��볣������ʽ��֪Ka��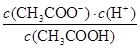 ��2��10-9/��c��0.02����
��2��10-9/��c��0.02����
���㣺����ƽ�ⳣ�������������ƽ��״̬��Ӱ�죻ԭ���ԭ�������֣���Һ������Ũ�ȴ�С�Ƚϣ��Լ���ҺpH�͵��볣�����йؼ����


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��Ҫ��������и�С�⣺
��Ҫ��������и�С�⣺

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ĵ�ʡ�Ű���ѧ�߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
��Ҫ��������и�С��
��1����д���Ƶĺ�������Ų�ʽ
��2�����������ļ۵��ӹ����ʾʽ
��3����д������һ������̼ԭ�ӵķ��� 
��4����д�������Ц� ���ľ������ͣ�������ɼ���ԭ�ӹ����
���ľ������ͣ�������ɼ���ԭ�ӹ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ���Ĵ�ʡ������ѧ�߶�10���¿���ѧ�Ծ� ���ͣ������
��6�֣���Ҫ��������и�С��
(1) д��Cu�ĵ����Ų�ʽ
(2) ����Ca��ԭ�ӽṹʾ��ͼ ��
(3) д��Se�ļ����Ų�ʽ
(4) д��Mn�ļ۵����Ų�ʽ
(5) ����Nԭ�ӵĵ����Ų�ͼ
��6��Znλ�����ڱ��� ������ ��������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���㽭ʡ�����ڶ����¿���ѧ�Ծ��������棩 ���ͣ�������
(13��)��Ҫ��������и�С�⡣
(1)��CO2������ȼ�ϼ״��ķ�Ӧԭ����CO2(g)+3H2(g) CH3OH(g)+H2O(g)��ijЩ��ѧ���ļ����������±���
CH3OH(g)+H2O(g)��ijЩ��ѧ���ļ����������±���
|
��ѧ�� |
C��C |
C��H |
H��H |
C��O |
C=O |
H��O |
|
����/kJ��mol-1 |
348 |
413 |
436 |
358 |
750 |
463 |
���㷴Ӧ������Ӧ���ʱ��H=_______________________
д��������Ӧ��ƽ�ⳣ������ʽK=__________________���������¶ȣ���ƽ�ⳣ��K________(�����С�����䡱)���÷�Ӧ�ġ�S______0(�>����<����=��)���� _________(��ϸߡ��ϵ͡�)�¶��������ڸ÷�Ӧ�Է����С�
(2)��25���£���Ũ�Ⱦ�Ϊ0��01 mol・L-1��MgCl2��AlCl3�����Һ����μ��백ˮ��������__________����(�ѧʽ)�����ɸó��������ӷ���ʽΪ________________��
����֪25��ʱKsp[Mg(OH)2]=1.8��10-11��Ksp[Al(OH)3]=3��10-34����
(3)ij�¶�(t��)ʱ�����0.01mol��L-1��NaOH��Һ��pH��11���ڴ��¶��£���pH��2��H2SO4��ҺVaL��pH��12��NaOH��ҺVbL��ϣ������û��ҺΪ���ԣ���Va�UVb�� ��
(4)��25��ʱ����cmol��L-1�Ĵ�����Һ��0.02mol��L-1NaOH��Һ�������Ϻ���Һ�պó����ԣ��ú�c�Ĵ���ʽ��ʾCH3COOH�ĵ��볣��Ka=____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�츣��ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��18�֣��±�ΪԪ�����ڱ��е�һ���֣������г���11��Ԫ�������ڱ��е�λ�ã���Ҫ��������и�С�⡣

(1) ��ѧ��������õ�Ԫ���� ����Ԫ�ط��Ż�ѧʽ����ͬ����
�ǽ�������ǿ��Ԫ���� ��
��������ǿ�ĵ�����ˮ��Ӧ�����ӷ���ʽ��
��
(2) �٢ۢ�����Ԫ�ص�����������Ӧ��ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ��
(3) �٢ڢ�����Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳���� �� �� ��
(4) ijԪ�ص�����������Ӧ��ˮ����������ᷴӦ�����κ�ˮ�����ܺͼӦ
�����κ�ˮ����Ԫ�ص��������������ᷴӦ�����ӷ���ʽΪ
��
���Ԫ�غ͢��Ԫ���γɵĻ��������Һ�У������μӰ�ˮ��������������ʵ�������� ���йط�Ӧ�Ļ�ѧ����ʽΪ ����5����Ԫ���γɵĵ�����Ũ���ᷢ����ѧ��Ӧ�Ļ�ѧ����ʽΪ
��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com