
| | A | B | C | D |
| 强电解质 | HBr | FeCl3 | H2SO4 | Ca(OH)2 |
| 弱电解质 | HF | HCOOH | BaSO4 | HI |
| 非电解质 | NH3 | Cu | H2O | C2H5OH |
 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源:不详 题型:填空题
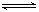 H++A-,其电离常数表达式 Ka= c(H+)·c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5
H++A-,其电离常数表达式 Ka= c(H+)·c (A-)/ c (HA)(各浓度为平衡时浓度)。该常数与浓度、压强无关,只是温度的函数。25℃,醋酸的Ka=1.76×10-5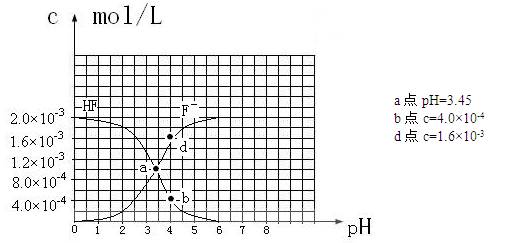
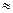 ,列式并说明得出该常数的理由 。
,列式并说明得出该常数的理由 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.因为NaHCO3溶于水后, 不能完全电离成H+和 不能完全电离成H+和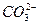 ,所以NaNCO3属于弱电解质 ,所以NaNCO3属于弱电解质 |
| B.弱电解质溶液的导电性一定比强电解质溶液的导电性差 |
| C.浓度相同(即单位体积内含有的分子数相同)的HCl和CH3COOH,前者导电能力比后者强,CH3COOH肯定是弱电解质 |
| D.在熔融状态下不能电离的电解质就是弱电解质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.:烧碱, | B.NH3.H2O, |
| C.SO3, | D.铁片,(E)食盐水,(F)甲烷, |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若弱酸HA的电离常数大于弱酸HB的电离常数,则同浓度钠盐溶液的碱性:NaA<NaB |
B.用广泛 试纸测得0.10mol·L 试纸测得0.10mol·L NH4Cl溶液的 NH4Cl溶液的 |
| C.HCl是强电解质,CH3COOH是弱电解质,所以盐酸溶液的导电性强于醋酸溶液 |
| D.将碳酸钾溶液蒸干,得到的固体物质是氢氧化钾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com