
【题目】能证明某烃分子里只含有一个碳碳双键的事实是( )
A. 该烃分子里碳氢原子个数比为1:2
B. 该烃能使酸性KMnO4溶液褪色
C. 该烃完全燃烧生成的CO2和H2O的物质的量相等
D. 该烃容易与溴水发生加成反应,且1mol该烃完全加成消耗1mol溴单质
科目:高中化学 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl﹣、NH4+、Mg2+、CO32﹣、Ba2+、SO42﹣ . 将该混合物溶于水后得澄清溶液,现取3份100mL该溶液分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
1 | 加AgNO3溶液 | 有白色沉淀生成 |
2 | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
3 | 加足量BaCl2溶液,反应后进行( )、( )、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
试回答下列问题:
(1)根据实验1~3判断混合物中一定不存在的离子是;
(2)写出实验3中的空格处的实验操作;
(3)根据实验对Cl﹣是否存在的判断是(填“一定存在”、“一定不存在”或“不能确定”);
(4)溶液中K+是否存在?(填“一定存在”、“一定不存在”或“不能确定”);若“一定存在”,则K+物质的量浓度的范围(若“一定不存在”或“不能确定”不填此空).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中选择的仪器正确的是:①分离汽油和氯化钠溶液 ②从含Fe3+的自来水中到蒸馏水③分离氯化钾和二氧化锰混合物 ④从氯化钠溶液中得到氯化钠晶体

A. ①-丁 ②-丙 ③-甲 ④-乙 B. ①-乙 ②-丙 ③-甲 ④-丁
C. ①-丁 ②-丙 ③-乙 ④-甲 D. ①-丙 ②-乙 ③-丁 ④-甲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,其物理性质与NaCl极为相似.相关转化关系如图所示,下列说法不正确的是( ) 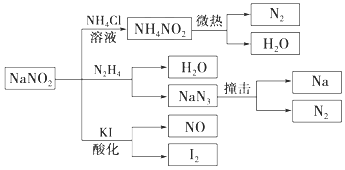
A.NaNO2在水中的溶解性大于NH4NO2
B.NaNO2与N2H4反应中,NaNO2是氧化剂
C.可用KI,淀粉和食醋鉴别NaNO2和NaCl
D.分解NaN3盐每产生1 mol N2 转移6 mol e﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国古代四大发明之一﹣﹣黑火药,它的爆炸反应为:2KNO3+3C+S ![]() A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为 . 除K、S外第一电离能从大到小的顺序为 .
②在生成物中,A的晶体类型为 , 含极性共价键的分子的中心原子轨道杂化类型为 .
③CN﹣与N2互为 , 推算HCN分子中σ键与π键数目之比 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】速力菲(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物。该药品不溶于水但能溶于人体中的胃酸。某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:
![]()
试回答下列问题:
(1)试剂1是______________,试剂2是_______________,加入新制氯水后溶液中发生的离子反应方程式是___________________________________________,_____________________________________;
(2)加入试剂2后溶液颜色由淡黄色转变为淡红色的原因可能是:_____________________。
(3)该同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗?_______________。若你认为合理,请说明理由(若你认为不合理,该空不要作答) ;若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不要作答)________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同温度下,将2mol X,2mol Y分别充入到不同体积的容器中,发生反应:X(g)+Y (g)mZ(g)△H,所得Z的平衡浓度如表所示,下列说法正确的是( )
| 1 | 2 | 3 |
200 |
|
|
|
300 | 2.4 | 1.2 | 0.8 |
400 | 2.0 | 1.0 |
|
A.m=2,△H>0
B.300℃时,该反应平衡常数 K=9
C.在3L容器中进行反应,达到平衡的时间:400℃>200℃
D.200℃,2L容器中反应达平衡后,再充入2 mol Z,平衡时 Z 的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,将A和B各0.32mol充入恒容密闭容器中,发生反应:A(g)+B(g)2C(g)△H=﹣a kJmol﹣1(a>0),反应过程中测定的数据如表,下列说法正确的是( )
t/min | 0 | 2 | 4 | 7 | 9 |
n(B)/mol | 0.32 | 0.24 | 0.22 | 0.20 | 0.20 |
A.若起始时向容器中充入0.64 mol C,则达平衡时吸收的热量为0.12a kJ
B.恒温,如果压缩容器体积,B的浓度和体积分数均不变
C.若起始时向容器中充入 0.64 mol A 和 0.64 mol B,则达平衡时 n(C)<0.48 mol
D.恒温、恒容,向平衡体系中再充入0.32 mol A,再次平衡时,B的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种具有耐高温、抗冲击、导热性好等优良性质的物质,被广泛应用于电子工业、陶瓷工业。在一定条件下,氮化铝可通过如下反应合成:![]() 。下列叙述正确的是
。下列叙述正确的是
A. 在该反应中,N2是还原剂,Al2O3是氧化剂
B. 在该反应中,每当生成2mol AlN,N2失去6mol电子
C. 氮化铝中氮元素的化合价为-3价
D. AlN既是氧化产物又是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com