
 的化合物N5AsF6,下列叙述错误的是
的化合物N5AsF6,下列叙述错误的是A.N 共有34个核外电子 共有34个核外电子 |
B.N 中氮-氮原子间以共用电子对结合 中氮-氮原子间以共用电子对结合 |
| C.化合物N5AsF6中As化合价为+1 |
| D.化合物N5AsF6中F化合价为-1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.直线形 sp杂化 | B.三角形 sp2杂化 |
| C.三角锥形 sp2杂化 | D.三角锥形 sp3杂化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.把铜片和铁片用导线连接后一起插入三氯化铁溶液中,在铜片表面出现一层铁 |
| B.取5mL 0.1 mol·L-1 FeCl3溶液,滴加0.1 mol·L-1 KI溶液5~6滴,再加入少量KSCN溶液,溶液呈红色,说明该反应有一定的限度 |
| C.硫酸与碳酸氢钠溶液混合产生无色气体,证明非金属性S>C |
| D.水的沸点较高是因为水分子中的氢氧键键能较大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.正四面体,非极性分子 | B.平面三角形,非极性分子 |
| C.四面体,极性分子 | D.平面三角形,极性分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CS2分子的立体构型为V形 |
B.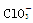 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.SF6中有每个原子均满足最外层8电子稳定结构 |
D.SiF4和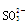 的中心原子均为sp3杂化 的中心原子均为sp3杂化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯化硼液态时能导电而固态时不导电 | B.氯化硼加到水中使溶液的pH升高 |
| C.氯化硼分子呈正三角形,属非极性分子 | D.氯化硼B-Cl之间是sp3形成的σ键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com