



| 132×6.1% |
| 1 |
| 132×12.1% |
| 16 |
| 2×9+2-8 |
| 2 |
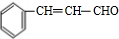 ,肉桂醛氧化得到X,X为
,肉桂醛氧化得到X,X为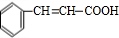 ,与溴发生加成反应后生成F,F为
,与溴发生加成反应后生成F,F为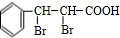 ,据此解答.
,据此解答.| 132×6.1% |
| 1 |
| 132×12.1% |
| 16 |
| 2×9+2-8 |
| 2 |
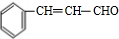 ,肉桂醛氧化得到X,X为
,肉桂醛氧化得到X,X为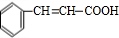 ,与溴发生加成反应后生成Y,Y为
,与溴发生加成反应后生成Y,Y为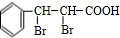 ,
,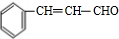 ,支链中含有碳碳双键、醛基,
,支链中含有碳碳双键、醛基,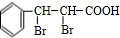 ,不存在双键,不能发生加聚反应,含有苯环,可以发生加成反应,含有-Br,可以发生水解反应与消去反应,
,不存在双键,不能发生加聚反应,含有苯环,可以发生加成反应,含有-Br,可以发生水解反应与消去反应,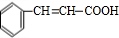 ,与乙醇发生酯化反应,反应方程式为:
,与乙醇发生酯化反应,反应方程式为: ,
, ;
;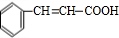 的同分异构体中,属于酯类且苯环上只有一个取代基,有如下4种:
的同分异构体中,属于酯类且苯环上只有一个取代基,有如下4种: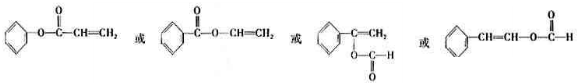


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
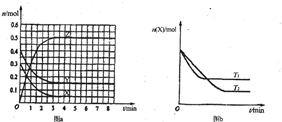 (2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )
(2010?诸城市模拟)T0℃时,在2L的密闭容器中发生反应:aX(g)+bY(g)?cZ(g),各物质的物质的量随时间变化的关系如图a所示.其他条件相同,温度分别为T1℃、T2℃时发生反应,X的物质的量随时间变化的关系如图b所示.下列叙述不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com