
| A、pH=6的纯水:c(OH-)<c(H+) |
| B、0.1mol?L-1的(NH4)2SO4溶液:c(NH4+)>c(SO42-)>c(H+) |
| C、常温下,pH=7的醋酸与醋酸钠的混合溶液:c(CH3COO-)>c(Na+) |
| D、常温下,pH=2的一元酸和pH=12的一元强碱等体积混合后所得溶液:c(OH-)=c(H+) |


科目:高中化学 来源: 题型:
| A、①②④⑤⑧ | B、②③⑤⑦⑧ |
| C、②③④⑦⑧ | D、全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有乙烷 |
| B、一定有甲烷 |
| C、一定没有甲烷 |
| D、不一定有甲烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
已知:NH2COO-+2H2O?HCO3-+NH3?H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )| A、无法判断T1和T2的大小关系 |
| B、T1℃时,第6min反应物转化率为6.25% |
| C、T2℃时,0~6min ν(NH2COO-)=0.3mol?L-1?min-1 |
| D、往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 向FeCl2溶液中加入几滴KSCN溶液,观察溶液颜色 | 检验FeCl2溶液是否已变质 |
| B | 将Cl2通入NaBr溶液中 | 比较氯气与溴的氧化性强弱 |
| C | 用冰水冷却铜与浓硝酸反应生成的气体 | 研究温度对化学平衡的影响 |
| D | 直接将CuCl2溶液加热蒸干 | 制取无水CuCl2固体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
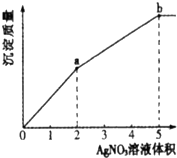 往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )
往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )| A、KSP(AgCl)<KSP(AgI) |
| B、c( Cl-):c( I-)=3:2 |
| C、m( AgCl ):m( AgI )=2:3 |
| D、a~b段产生黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验前 | 实验后 | |
| 甲的质量/g | 101.1 | 103.8 |
| 乙的质量/g | 82.0 | 88.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a电极反应式:SO2+2H2O-2e-═SO42-+4H+ |
| B、b极与电源的正极相连 |
| C、离子交换膜c为阳离子交换膜 |
| D、气体W为氧气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com