
有关热化学方程式书写与对应表述均正确的是( )
A.已知2C(s)+O2(g)=2CO(g) △H=-221 kJ·mol-1, 则可知C的标准燃烧热为110.5 kJ·mol-1
B.在101KPa下氢气的标准燃烧热△H =-285.5 kJ·mol-1,
则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) △H = +285.5 kJ·mol-1
C.稀硫酸与0.1 mol/LNaOH溶液反应:H+(aq)+OH-(aq) = H2O(l) △H = -57.3 kJ·mol-1
D.密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量。则Fe(s)+S(g)=FeS(s) △H= - 95.6 kJ·mol-1
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源:2016-2017学年江西省高一12月月考化学卷(解析版) 题型:选择题
某份铁铝合金样品均分为两份,一份加入足量盐酸,另一份加入足量NaOH溶液,同温同压下产生的气体体积比为3∶2,则样品中铁、铝物质的量之比为( )
A.3∶2 B.2∶1
C.3∶4 D.4∶3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高一12月月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3- =CaCO3↓+ H2O
B.氯化铝溶液中加入过量氨水:Al3++4NH3•H2O =AlO2-+4NH4++2H2O
C.碳酸钙溶于醋酸CaCO3+2H+=Ca2++CO2↑+H2O
D.氯化亚铁溶液中通入氯气:Fe2++Cl2=Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:实验题
某常用的血液抗凝剂由(NH4)2C2O4和Na2C2O4组成,为确定其成分,某同学进行如下实验:
①氮元素测定:精确称取a g样品,加适量蒸馏水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量浓NaOH溶液,加热装置A产生水蒸气,装置B中产生的氨气全部吹出,用V1mLc1mol/L的硫酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol/LNaOH标准溶液过剩的H2SO4,到终点时消耗V2mLNaOH溶液。
②C2O42-离子的测定:取实验①B装置中剩余溶液于锥形瓶中,先用稀硫酸酸化,再用0.1000mol/L的酸性KMnO4溶液滴定,终点时消耗酸性KMnO4溶液V3mL。
③计算:根据实验①计算氮元素的含量,根据②计算C2O42-的含量,从而得到样品中(NH4)2C2O4和Na2C2O4的比例。完成下列问题:
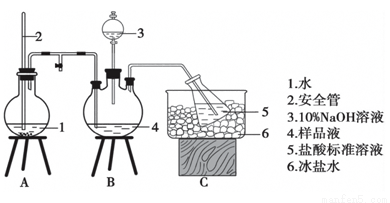
(1)装置A中长玻璃管的作用是 。
(2)用NaOH标准溶液滴定过剩H2SO4时, NaOH标准溶液盛装在 中(填仪器名称)。
(3)样品中氮元素的质量分数表达式为 。
(4)实验②中发生的离子方程式为 。用酸性高锰酸钾溶液滴定时终点现象为 。
(5)实验②中滴定开始和结束时,滴定管的读数如图所示,则所用酸性KMnO4溶液体积V3= mL
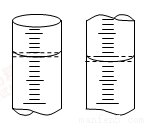
(6)下列操作可能使实验②测定结果偏低的是 。
A.滴定管在注入溶液前用蒸馏水洗后未用标准溶液润洗
B.开始时酸式滴定管尖嘴部分有气泡,滴定过程中消失
C.滴定前仰视滴定管读数,滴定后平视滴定管读数
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y 各0.16 mol充入10 L 恒容密闭容器中,发生反应
X(g)+ Y(g) 2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
2Z(g) △H < 0,一段时间后达到平衡。反应过程中测定的数据如下表。下列说法正确的是 ( )
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10-5 mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南浏阳一中等两校高二12月联考化学卷(解析版) 题型:选择题
下列说法中,可以说明恒容密闭容器中的反应:P(g)+Q(g) R(g)+S(g)在恒温下已达平衡状态的是 ( )
R(g)+S(g)在恒温下已达平衡状态的是 ( )
A.反应容器内压强不随时间变化
B. P和S的生成速率相等
C.反应容器内P、Q、R、S四者物质的量浓度为1:1:1:1
D.反应容器内总物质的量不随时间而变化
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:计算题
将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的物质的量为________mol,NO2的物质的量为________mol。
(2)待产生的气体全部释放后,向溶液中加入VmL、amol·L-1的NaOH溶液,恰好使溶液中的Cu2+全部转化成沉淀,则原硝酸溶液的浓度为________mol·L-1。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO3,至少需要30%的双氧水_______g。
(书写计算过程)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(解析版) 题型:选择题
已知甲、乙、丙和X是四种中学化学中常见的物质,其转化关系如下图,则甲和X不可能是( )

A.甲为C,X是O2 B.甲为SO2,X是NaOH溶液
C.甲为Cl2,X为Fe D.甲为Al,X为NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2017届贵州省高三上联考四化学试卷(解析版) 题型:选择题
短周期元素Q、W、X、Y、Z的原子序数依次增大,X元素的焰色反应呈黄色,Q原子的最外层电子数是其内层电子数的2倍,W、Z原子的最外层电子数相同,Z的核电荷数是W的2倍,Y是地壳中含量最多的金属元素。下列说法不正确的是
A. 工业上常用电解的方法制备X、Y的单质
B. 元素Q和Z能形成QZ2型的共价化合物
C. 原子半径的大小顺序:r(X)>r(Y)>r(W)>r(Q)
D. 元素X、Y、Z的最高价氧化物对应的水化物之间能相互发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com