
| △ |
| △ |
| 250-350℃ |
| Cu |
| 250-350℃ |
| Cu |
| 操作方法及所用试剂 | 实验现象 |
洗气、水 洗气、水 |
酸性高锰酸钾溶液褪色 酸性高锰酸钾溶液褪色 |
| 12 |
| 12 |
| 3 |
| 1 |
| 8 |
| 16 |
| 催化剂 |
| △ |
| △ |
| 12 |
| 12 |
| 3 |
| 1 |
| 8 |
| 16 |
| △ |
| △ |
| 250-350℃ |
| Cu |
| 250-350℃ |
| Cu |
| 操作方法及所用试剂 | 实验现象 |
| 洗气、水 | 酸性高锰酸钾溶液褪色 |


科目:高中化学 来源: 题型:
 由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中甲、乙、丙是单质,X、Y是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.以下判断错误的是( )
由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中甲、乙、丙是单质,X、Y是化合物.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质.以下判断错误的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
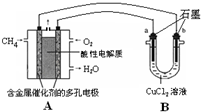 (2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.
(2013?焦作一模)开发新能源,使用清洁燃料,可以达到提高能效、减少污染的目的.| 1 |
| 3 |
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修5) 2009-2010学年 第22期 总第178期 人教课标版(选修5) 题型:058
测定某有机化合物甲的结构,进行如下实验:
[分子式的确定]
(1)经测定有机物甲由C、H、O三种元素组成,元素的质量比为12∶3∶8,其蒸气密度是H2密度的23倍.根据价键理论,预测甲的可能结构并写出结构简式________.
[结构式的确定]
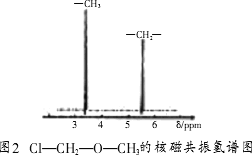
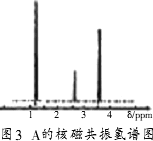
(2)核磁共振氢原子光谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(图2).经测定,有机物甲的核磁共振氢谱示意图如图3,则甲的结构简式为________.
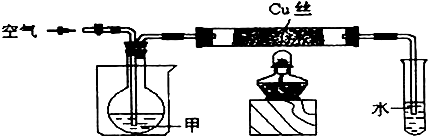
[性质探究]将温度控制在400℃以下,根据图4,按要求完成实验.(已知甲的沸点为78.5℃)
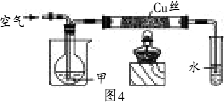
(3)在通入空气的条件下进行实验Ⅰ.
甲的名称是________,加入药品后的操作依次是________.
a.打开活塞
b.用鼓气球不断鼓入空气
c.点燃酒精灯给铜丝加热
(4)在停止通入空气的条件下进行实验Ⅱ.
①关闭活塞,为使甲持续进入反应管中,需要进行的操作是________;
②甲蒸气进入反应管后,在铜作催化剂及
查看答案和解析>>
科目:高中化学 来源:长乐二中2007年高考化学实验预测题 题型:058
| |||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com