
【题目】肉桂酸的一种合成路线如下:
(1)烃A的名称为 . 反应①中B的产率偏低,其原因是 .
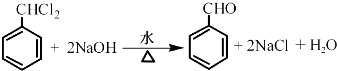
(2)反应②的化学方程式为 .
(3)反应③的反应类型是 .
(4)肉桂酸的结构简式为 .
(5)反应③的产物同分异构体有多种,其中苯环上直接有一个甲基的酯类化合物有种.
【答案】
(1)甲苯;反应中有一氯取代物和三氯取代物生成
(2)
(3)加成反应
(4)![]()
(5)9
【解析】解:A与氯气在光照条件下与氯气发生取代反应生成B,B发生卤代烃的水解反应,再脱去1分子水得到 ![]() ,则A为
,则A为 ![]() ,B为
,B为 ![]() ,
, ![]() 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 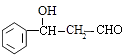 ,分子式为C9H10O2 , 对比
,分子式为C9H10O2 , 对比 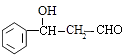 的结构与加热后的产物的分子式可知,
的结构与加热后的产物的分子式可知, 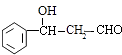 脱去1分子水得到C9H8O,应是发生消去反应生成C9H8O,则C9H8O为
脱去1分子水得到C9H8O,应是发生消去反应生成C9H8O,则C9H8O为 ![]() ,
, ![]() 与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为
与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为 ![]() ,(1)烃A为
,(1)烃A为 ![]() ,名称为甲苯,步骤Ⅰ中反应中有一氯取代物和三氯取代物生成,B的产率往往偏低, 所以答案是:甲苯;反应中有一氯取代物和三氯取代物生成;(2)步骤②反应的化学方程式为
,名称为甲苯,步骤Ⅰ中反应中有一氯取代物和三氯取代物生成,B的产率往往偏低, 所以答案是:甲苯;反应中有一氯取代物和三氯取代物生成;(2)步骤②反应的化学方程式为 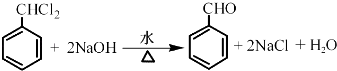 ,所以答案是:
,所以答案是:  ;(3)反应③
;(3)反应③ ![]() 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 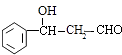 ,反应类型是加成反应,所以答案是:加成反应;(4)根据分析可知,肉桂酸的结构简式为:
,反应类型是加成反应,所以答案是:加成反应;(4)根据分析可知,肉桂酸的结构简式为: ![]() ,所以答案是:
,所以答案是: ![]() ;(5)
;(5) 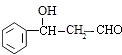 的同分异构体有多种,其中苯环上有一个甲基的酯类化合物,有2个侧链为﹣CH3、﹣CH2OOCH,或﹣CH3、﹣OOCCH3 , 或﹣CH3、﹣COOCH3 , 各有邻、间、对3种,共有9种,
的同分异构体有多种,其中苯环上有一个甲基的酯类化合物,有2个侧链为﹣CH3、﹣CH2OOCH,或﹣CH3、﹣OOCCH3 , 或﹣CH3、﹣COOCH3 , 各有邻、间、对3种,共有9种,
所以答案是:9.


科目:高中化学 来源: 题型:
【题目】如图所示的实验装置,丙为酚酞溶液润湿的淀粉碘化钾试纸,m、n为夹在滤纸两端的铂夹.丁为直流电源,x、y为电源的两极.G为电流计,电极均为石墨电极.闭合K2、断开K1 , 一段时间后,A极产生的气体体积为44.8ml、B极产生的气体体积为22.4ml(都已换算成标况下的体积),回答下列问题: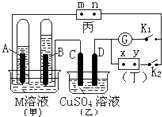
(1)M溶液可能是(填序号).
A.KCl溶液
B.Ba(OH)2溶液
C.KNO3溶液
D.CuCl2溶液
(2)乙池中盛有足量的硫酸铜溶液,D电极上的电极反应式为 , 此时向溶液中加入可以使溶液完全复原.
(3)滤纸丙上m点附近变为色,n点附近变为色,
(4)继续电解一段时间后,甲池中A、B极均部分被气体包围,此时闭合K1 , 断开K2 , 发现电流计G指针发生偏转,若M为硫酸溶液,写出B电极上发生的反应式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下列实验方法制备气体,合理而又实用的是( )
A.锌粒与稀硝酸反应制备H2
B.将饱和氨水滴加到新制的生石灰制NH3
C.亚硫酸钠与稀硫酸反应制备SO2
D.大理石与浓硫酸反应制备CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含碘元素。从海带中提取碘有如下步骤:①通入适量Cl2;②将海带灼烧成灰后加蒸馏水搅拌;③加CCl4振荡;④过滤。合理的操作顺序是( )
A.①②③④
B.②①③④
C.①③②④
D.②④①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期的非金属元素(其单质也可分别用A、B、C、D表示),四种元素的原子序数按B、D、C、A顺序增大,D、C元素在周期表中位置相邻。在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙化合物,C和D化合可得丁。已知乙、丙两个分子中各含有10个电子,并且甲、乙、丙、丁、戊有如下的变化关系:
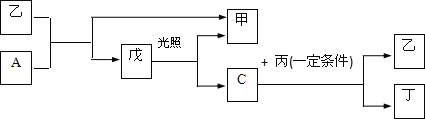
请回答下列问题:
(1)甲的浓溶液与一种黑色粉末共热可得A。实验室制备A的离子方程式为:__________________;
(2)B元素在周期表中的位置是______________,B在A中燃烧的现象是____________;
(3)写出下列反应的化学方程式:
①C +丙:_____________________________________________;
②丙+丁→D + 乙:___________________________________________;
③A +丙→D + 甲:_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CCl4和蒸馏水都是无色液体,请按下列要求用实验方法鉴别:
(1)只允许用一种试剂:用两支试管分别取出少量的CCl4和蒸馏水,然后分别加入少量的单质碘,振荡,呈紫红色的液体是__________,呈棕黄色的液体是__________。
(2)不用任何试剂:用试管取出少量的其中一种液体,再加入另外一种液体,下层液体是__________,上层液体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置用于实验室制取氨气并检验氨气的某一化学性质,其中能达到实验目的是( )
A.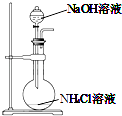 用装置图制取氨气
用装置图制取氨气
B.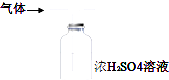 用装置图除去氨气中的水蒸气
用装置图除去氨气中的水蒸气
C.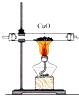 用装置图验证氨气具有还原性
用装置图验证氨气具有还原性
D.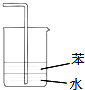 用装置图吸收氨气
用装置图吸收氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL密度为1.40g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况).向反应后的溶液中加入1.0mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
A.该浓硝酸中HNO3的物质的量浓度是12.0 mol/L
B.该合金中铜与镁的物质的量之比是2:1
C.NO2和N2O4的混合气体中,N2O4的体积分数是20%
D.得到2.54g沉淀时,加入NaOH溶液的体积是6.0 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com