
分析 由信息可知,加入铁反应还生成氢气,则一定量的CuO粉末与0.5L稀硫酸充分反应,发生CuO+H2SO4═CuSO4+H2O,且硫酸剩余,然后加Fe,发生Fe+CuSO4═FeSO4+Cu、Fe+H2SO4═FeSO4+H2↑,然后结合气体的体积及质量差计算.
解答 解:氧化铜能与硫酸反应生成硫酸铜和水,生成的硫酸铜能与铁反应生成硫酸亚铁和铜,生成的铜附着在铁的表面,铁能与硫酸反应生成氢气,并收集到224mL气体(标准状况),所以氢气的物质的量为:0.01mol,质量为:0.02g,设生成0.02g氢气需要铁的质量为x则有
Fe+H2SO4═FeSO4+H2↑
56 2
x 0.02g
$\frac{56}{x}=\frac{2}{0.02}$,
x=0.56g,
与硫酸铜反应的铁的质量为50g-0.56g=49.44g,反应后铁棒的质量为50.24g,说明铁与硫酸铜反应时增重的质量为50.24g-49.44g=0.8g,设硫酸铜的质量为y,根据反应的化学方程式则有
Fe+CuSO4═FeSO4+Cu△m
56 160 64 8
y 0.8g
$\frac{160}{y}=\frac{8}{0.8g}$,
解得y=16g,
设氧化铜的质量为z.则有
CuO+H2SO4═CuSO4+H2O
80 160
z 16g
$\frac{80}{z}=\frac{160}{16g}$,解得z=8g,
答:此CuO粉末的质量为8g.
点评 本题考查了金属活动性顺序的应用以及根据化学方程式的计算,注意发生的化学反应及反应中过量的分析是解答本题的关键,差量法计算为解答的难点.


科目:高中化学 来源: 题型:选择题
| A. | 锌为负极,锌发生氧化反应 | |
| B. | 铜为正极,电极反应式:2H++2e-═H2↑ | |
| C. | 电解质溶液中,SO42-向正极方向移动 | |
| D. | 外电路电子流入的一极为正极,电子流出的一极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属原子间以共价键结合形成的物质都是共价化合物 | |
| B. | Na2CO3和CaCl2中化学键类型(离子键、共价键)完全相同 | |
| C. | 阴、阳离子通过静电引力而形成的化学键叫做离子键 | |
| D. | 含有离子键的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
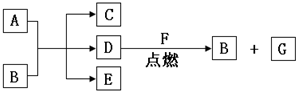
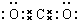 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g 46%的乙醇水溶液含有的氧原子数为0.4NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液1.0L,含有OH-数目0.2NA | |
| C. | 4.6g C2H6O含有的C-H键总数一定为0.5NA | |
| D. | 常温下,0.1mol Cl2溶于水转移的电子数为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
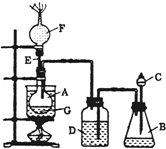 为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:
为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| B. | Fe Cl3溶液中加入足量的氨水:Fe3++3OH-=Fe (OH)3↓ | |
| C. | 钠与CuSO4溶液反应:2Na+Cu2+=Cu+2Na+ | |
| D. | 用小苏打治疗胃酸过多病:HCO3-+H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com