
(14 分) 一氧化碳被广泛应用于冶金工业和电子工业。
⑴高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H=a kJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H=b kJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H= kJ·mol-1(用含a、b 的代数式表示)。
⑵电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g) HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g) CH3OH(g) +CO(g) △H>0
CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:
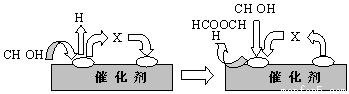
图中中间产物X的结构简式为 。
②在工业生产中,为提高CO的产率,可采取的合理措施有 。
⑶为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为 。

⑷某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。
上述两步中消耗CO的物质的量之比为 。
⑸为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为 。
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为 。

⑴(2a+b)/3 ⑵①HCHO ②升高温度,降低压强
⑶FeAl2O4+8H+=Fe2++2Al3++4H2O ⑷3:8
⑸①0.1mol(或0.1NA) ②CO+H2O-2e-=CO2+2H+ (每空2分,共14分)
【解析】
试题分析:⑴将“①×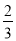 +②×
+②×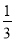 ”能得该方程式,根据盖斯定律可该反应热△H=(2a+b)/3 kJ·mol-1。
”能得该方程式,根据盖斯定律可该反应热△H=(2a+b)/3 kJ·mol-1。
⑵①CH3OH脱氢后生成HCHO;
②根据第一步和第二步的反应特点,可知“升高温度,降低压强”能提高CO的产率;
⑶根据“反应后混合物中的一种产物能与盐酸反应生产两种盐”说明该反应的反应物有FeAl2O4、盐酸,生成物有FeCl2、AlCl3、H2O,据此便可写出离子方程式。
⑷先确定发生的两步反应:3CO+Ni2O3=3CO2+2Ni,Ni+4CO=Ni(CO)4,则这两步中消耗CO的物质的量之比为3:8。
⑸①根据“PdCl2~Pd~2e-”,则每生成5.3gPd沉淀,反应转移电子数为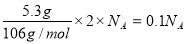 。
。
②CO在负极上发生氧化反应,据得失电子守恒有CO-2e―――CO2,再据电荷守恒有CO-2e――CO2+2H+,最后据原子守恒得CO+H2O-2e-=CO2+2H+。
考点:考查化学反应基本原理(反应热的计算、平衡移动原理、离子方程式的书写、氧化还原反应电子转移数的计算、电极反应式的书写等)。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.同时用食醋和酒烧菜,菜味更香
B.蔗糖溶液中加入银氨溶液水浴加热,有银镜生成
C.苯中碳碳键是介于C-C和C=C之间的一种特殊共价键
D.反应2CrO3 + 3CH3CH2OH +3H2SO4 = Cr2(SO4)3+3CH3CHO+6H2O可用于检验是否酒后驾驶,该反应中CrO3作氧化剂
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:填空题
(27分)(1)现有如下两个反应:①NaOH + HCl = NaCl + H2O;②Fe +H2SO4 = FeSO4 + H2 ↑
两反应中为放热反应的是 ,能设计成原电池的是 。(填序号)
(2)根据下图填空① 电子从 片流出,溶液中H+向 片移动。

② 正极的现象是 ,发生 反应(填写“氧化”或“还原”)。
③负极的电极方程式为
④ 若反应过程中有0.01mol电子发生转移,则生成的氢气在标准状况下的体积为 L。
(3)写出电解氯化铜溶液时,阴极的电极反应方程式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:选择题
决定化学反应速率的根本因素是
A.温度和压强 B.反应物的浓度
C.物质自身的性质 D.催化剂的加入
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列化学用语的书写,正确的是
A.氮气的电子式: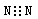 B.硫离子的结构示意图:
B.硫离子的结构示意图: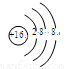
C.溴化钠的电子式: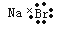 D.水分子的球棍模型:
D.水分子的球棍模型: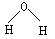
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三第三次调研测试化学试卷(解析版) 题型:选择题
一定条件下存在反应:C(s)+H2O(g) CO(g)+H2(g) △H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g) △H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。

容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1 ℃ | T2 ℃ | T1 ℃ |
起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2 molH2O |
下列说法正确的是
A.甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol·L-1·min-1
B.丙容器的体积V<0.5 L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)=0.4 mol,则T1< T2
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三第三次调研测试化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.向铁粉中加入足量稀硝酸:2Fe+6H+=2Fe3++3H2↑
B.向AlCl3溶液中滴加浓氨水至过量:Al3++4OH-=AlO2-+2H2O
C.向NaIO3溶液中加入适量NaHSO3溶液:IO3-+3HSO3-=I-+3SO42-+3H+
D.向NH4HCO3溶液中滴加过量NaOH溶液:NH4++HCO3-+2OH-=CO32-+NH3·H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三5月信息卷化学试卷(解析版) 题型:选择题
下列依据相关实验得出的结论正确的是
A.向溶液X中滴加盐酸无明显现象,再滴加BaCl2溶液有白色沉淀,则X中含有SO42-
B.向NaAlO2溶液中滴入NaHCO3溶液有白色沉淀,则AlO2-结合H+能力比CO32-强
C.向1 mL 1% NaOH溶液加入2 mL 2%的CuSO4溶液,振荡后滴加0.5 mL5%葡萄糖溶液,加热,未出现红色沉淀。证明葡萄糖中不含醛基
D.检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省泰州市姜堰区高二下学期期中考试 化学试卷(解析版) 题型:选择题
金银花中能提取出有很高药用价值的绿原酸(如下图),下列判断正确的是
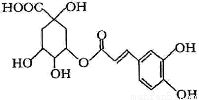
A.分子中有可能所有碳原子共平面 B.分子式为C16H18O9
C.分子中含有醚键 D.分子中有4个手性碳原子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com