
����Ŀ��ij��ȤС��̽��SO2���廹ԭFe3��������ʹ�õ�ҩƷ��װ������ͼ��ʾ������˵������������(����)
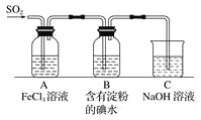
A.�ܱ���I���Ļ�ԭ������SO2��������B����ɫ��Һ��ɫ
B.װ��C������������SO2β������ֹ��Ⱦ����
C.Ϊ����֤A�з�����������ԭ��Ӧ������KMnO4��Һ���Ϻ�ɫ��ȥ
D.Ϊ����֤A�з�����������ԭ��Ӧ��������ϡ�����ữ��BaCl2��Һ��������ɫ����
���𰸡�C
��������
A. ���е��۵ĵ�ˮ��ͨ��SO2���壬�ᷢ����Ӧ��SO2��I2��2H2O===H2SO4��2HI������I2��Ӧ�����ģ����B����ɫ��Һ��ɫ��֤�����ʵĻ�ԭ�ԣ�SO2>I������A��ȷ��
B. SO2�Ǵ�����Ⱦ�����SO2���������壬������NaOH������Ӧ��SO2��2NaOH=Na2SO3��H2O�����Կ�����NaOH��Һ����β������ֹ��Ⱦ��������B��ȷ��
C. ��SO2��FeCl3��������Ӧ����A�м���KMnO4��Һ��������Ӧ��2KMnO4��5SO2�� 2H2O=K2SO4��2MnSO4��2H2SO4����Һ�Ϻ�ɫ��ȥ����SO2��FeCl3������Ӧ��SO2��2H2O��2FeCl3=H2SO4��2HCl��2FeCl2���������Һ�м������Ը��������Һʱ���ᷢ����Ӧ��MnO4-��5Fe2����8H+=Mn2���� 5Fe3����4H2O����Һ�Ϻ�ɫҲ��ȥ����˲�����֤A���Ƿ�����������ԭ��Ӧ����C����
D. ��A�з�����������ԭ��Ӧ��SO2��2H2O��2FeCl3=H2SO4��2HCl��2FeCl2����Һ�к������ᣬ��������ϡ�����ữ��BaCl2��Һʱ���ᷢ����Ӧ��H2SO4�� BaCl2=BaSO4����2HCl��������ɫ��������û�з���������ԭ��Ӧ������������HCl>H2SO3��������Һ�м�����ϡ�����ữ��BaCl2��Һʱ����������ɫ��������D��ȷ��
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CH4��Cl2�ķ�Ӧ(��ͼ��ʾ)��������ȷ���ǣ� ��
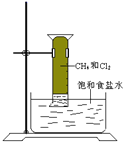
A.�÷�Ӧ����ȡ����Ӧ
B.�÷�Ӧ�������ǹ���
C.�÷�Ӧ��������������
D.�÷�Ӧ����������Ͳ��������ɫ��dz������������״Һ�Σ���Ͳ��Һ������������������ˮ�����о�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��д��ȷ����
A. HCO3�ĵ��뷽��ʽ��HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. ��ĭ�������ԭ����Al3++3HCO3- ![]() Al(OH)3��+3CO2��
Al(OH)3��+3CO2��
C. NH4Cl����D2O��NH4++D2O![]() NH3��D2O+H+
NH3��D2O+H+
D. Na2S�Լ���ԭ��S2-+2H2O![]() H2S+2OH-
H2S+2OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС�����ۼס��ҡ���������������װ�õ��й��÷�������˵������ȷ���ǣ�������
A.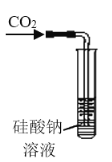 ������֤��̼�ķǽ����Աȹ�ǿ
������֤��̼�ķǽ����Աȹ�ǿ
B.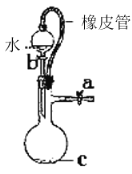 ��Ƥ�ܵ���������ʹˮ˳������
��Ƥ�ܵ���������ʹˮ˳������
C. ��ͼʾ�ķ������ܼ���װ�õ�������
��ͼʾ�ķ������ܼ���װ�õ�������
D. �ȴ����ڽ�������CO2���ٴ����ڽ��������ռ�NO
�ȴ����ڽ�������CO2���ٴ����ڽ��������ռ�NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A. �ϳɰ���Ӧ���ȣ����õ��¿�����߰�����������
B. �����£���pH��4�Ĵ�����Һ��ˮϡ�ͣ���Һ���������ӵ�Ũ�Ⱦ�����
C. ��Ӧ4Fe(OH)2(s)��2H2O(l)��O2(g)===4Fe(OH)3(s)���������Է����У��÷�Ӧ����H<0
D. ��һ�ݻ��ɱ���ܱ������з�Ӧ2SO2(g)��O2(g)![]() 2SO3(g)��ƽ������¶Ȳ��䣬��С�����ƽ�������ƶ���
2SO3(g)��ƽ������¶Ȳ��䣬��С�����ƽ�������ƶ���![]() ��ֵ����
��ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϲ�����������ȥ��������(��Ҫ�ɷ�ΪFe2O3��FeO��SiO2��Al2O3����������������) ��ȡ��ˮ����������(FeSO4��7H2O) ���������£�
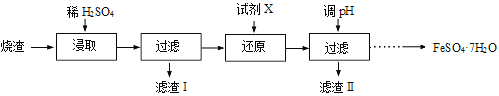
��1����ȡʱ����Һ�е�Fe2+�ױ������е�O2�����������ӷ���ʽΪ �������������ȡ���ʵĴ�ʩ�� ������ĸ����
A������������ B�����������Ũ�� C���ʵ������¶�
��2����ԭʱ���Լ�X����������ҺpH�ı仯��ͼ��ʾ�����Լ�X������ ������ĸ����
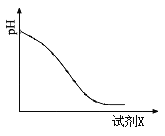
A��Fe�� B��SO2 C��NaI
��ԭ����ʱ����Һ�е���Ҫ�������� ��
��3����������Ҫ�ɷֵĻ�ѧʽΪ ���ɷ���������������Һ�õ���Ʒ�����еIJ����� �� ���ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ѣ�DME������Ϊ��21���͵����ȼ�ϡ����ɺϳ����Ʊ������ѵ���Ҫԭ�����£�
�� CO(g)+2H2(g)![]() CH3OH(g) ��H 1=��90.7 kJ��mol-1
CH3OH(g) ��H 1=��90.7 kJ��mol-1
�� 2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1
CH3OCH3(g)+H2O(g) ��H 2=��23.5 kJ��mol-1
�� CO(g)+H2O(g)![]() CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1
CO2(g)+H2(g) ��H 3=��41.2kJ��mol-1
�ش��������⣺
��1����Ӧ3H2(g)��3CO(g)![]() CH3OCH3(g)��CO2(g) ��H��____kJ��mol-1��
CH3OCH3(g)��CO2(g) ��H��____kJ��mol-1��
���д�ʩ�У������CH3OCH3���ʵ���____��
A��ʹ�ú��ʵĴ��� B�������¶� C������ѹǿ
��2�����ϳ�����n(H2)/n(CO)=2ͨ��1 L�ķ�Ӧ���У�һ�������·�����Ӧ��4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ����____��
CH3OCH3(g)+H2O(g) ��H����CO��ƽ��ת�������¶ȡ�ѹǿ�仯��ϵ��ͼ1��ʾ������˵����ȷ����____��
A����H < 0
B��P1<P2<P3
C������P3��316��ʱ����ʼn(H2)/n(CO)=3����ﵽƽ��ʱ��COת����С��50��
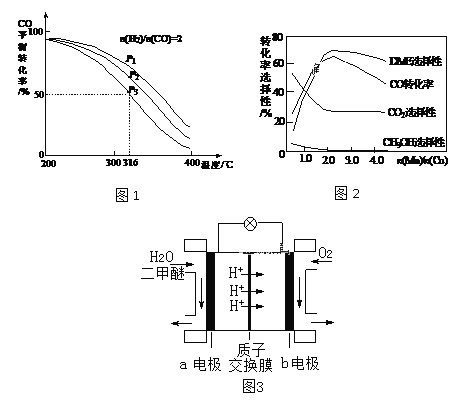
��3������һ�����͵Ĵ�������Ҫ�ɷ���Cu-Mn�ĺϽ𣩣�����CO��H2�Ʊ������ѡ��۲�ͼ2�ش����⡣������n(Mn)/n(Cu)ԼΪ____ʱ�������ڶ����ѵĺϳɡ�
��4��ͼ3Ϊ��ɫ��Դ��������ȼ�ϵ�ء��Ĺ���ԭ��ʾ��ͼ��b�缫�ĵ缫��ӦʽΪ____��
��5���״�Һ����ˮ���ƶ����ѵ�ԭ���ǣ�
CH3OH +H2SO4 �� CH3HSO4+H2O��
CH3 HSO4+CH3OH �� CH3OCH3+H2SO4��
��ϳ����Ʊ������ѱȽϣ��ù��յ��ŵ��Ƿ�Ӧ�¶ȵͣ�ת���ʸߣ���ȱ����____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2NO2(g)![]() 2NO(g)+O2(g)�����ݻ��̶����ܱ������н������ﵽƽ��״̬�ı�־��( )
2NO(g)+O2(g)�����ݻ��̶����ܱ������н������ﵽƽ��״̬�ı�־��( )
�ٵ�λʱ��������n mol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2��ͬʱ����2n mol NO
����NO2��NO��O2��ʾ�ķ�Ӧ����֮��Ϊ2:2:1��״̬
�ܻ���������ɫ���ٸı��״̬
�ݻ��������ܶȲ��ٸı��״̬
��������ѹǿ���ٸı��״̬
��������ƽ����Է����������ٸı��״̬
A.�٢ܢޢ�B.�ڢۢݢ�C.�٢ۢܢ�D.ȫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�òⶨ�к��ȵ�ʵ�鲽�����£�

������Ͳ��ȡ50mL0.50mol/L���ᵹ��С�ձ��У���������¶ȣ�
������һ��Ͳ��ȡ50mL0.55mol/L NaOH��Һ��������һ�¶ȼƲ�����¶ȣ�
�۽�NaOH��Һ����С�ձ��У���Ͼ��ȣ���û��Һ����¶ȡ�
�ش��������⣺
(1)д���÷�Ӧ���Ȼ�ѧ����ʽ����֪����lmolҺ̬ˮ�ķ�Ӧ��Ϊ��57.3kJ/mol��______________________��
(2)�ֽ�һ������ϡ����������Һ��ϡ����������Һ��ϡ��ˮ�ֱ�� 1L1mol/L����ǡ����ȫ��Ӧ���䷴Ӧ�ȷֱ�ΪH1��H2��H3����H1��H2��H3�Ĵ�С��ϵΪ________________________��
(3)�������������������Һ���ܶȶ���1g/cm3����֪�кͷ�Ӧ��������Һ�ı�����c=4.18J/(g����)��Ϊ�˼����к��ȣ�ijѧ��ʵ���¼���������
ʵ����� | ��ʼ�¶� | ��ֹ�¶� | |
���� | ����������Һ | �����Һ | |
1 | 20.0 | 20.2 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.4 | 20.6 | 23.6 |
4 | 20.1 | 20.3 | 26.9 |
���ݸ�ѧ����ʵ�����ݼ��㣬��ʵ���õ��к���H_____(�������һλС��)��
(4)�����60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������__________ (���ȡ�����ȡ�)�������к���__________(���ȡ�����ȡ�)��
(5)���ü������ȼƲ�������������������������Һ�кͷ�Ӧ�ķ�Ӧ�ȣ����д�ʩ�������ʵ�龫�ȵ�����_______��
A��������Һ��(��ȷ��0.01 mL)������Ͳ(��ȷ��0.1 mL)��ȡ��ӦҺ
B�����ٽ�����Һ��ϣ����ٽ��貢��¼����¶�
C�����ڡ���Ͳ֮�����������ʣ���ֹ������ʧ
D��������Ϊ500����¶ȼƴ�������Ϊ100����¶�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com