
| A.H3O+ | B.BF3 | C.CF2Cl2 | D.PCl5 |
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源:不详 题型:单选题
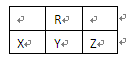
| A.X的氢化物比R的氢化物稳定 |
| B.原子半径大小顺序是Z>Y>X |
| C.Y、R形成的化合物YR2能使KMnO4溶液褪色 |
| D.X、Z可形成化合物XZ5,分子中各原子均满足最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④⑤ | B.②④⑥ | C.④⑤⑥ | D.③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XO32- | B.XO3- | C.XO42- | D.XO4- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 位置是 ,Na原子结构示意图为 ,其中三种主族元素的离子半径从大到小的顺序是 (用离子符号表示)
位置是 ,Na原子结构示意图为 ,其中三种主族元素的离子半径从大到小的顺序是 (用离子符号表示)  (用离子方程式表示)。
(用离子方程式表示)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com