

(1)左图。负极:__________;正极:____________________________,
总式:____________________________。
(2)右图。负极:__________;正极:____________________________,
总式:____________________________。
科目:高中化学 来源: 题型:
实验仪器和药品
灵敏电流计、铁架台、长20cm的木棒(绝缘棒)、粉笔、胶头滴管、铁丝、铜丝、无水乙醇、0.2mol?L-1的稀硫酸。
三、实验方案及操作步骤
1.按右图连接装置(灵敏电流计未画出)。
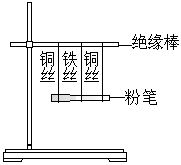
2.在粉笔上滴加无水乙醇,用电流计的两笔头分别接触两铜丝,然后再用两笔头接触铜丝和铁丝。
3.在粉笔上滴加0.2mol?L-1的稀硫酸,重复操作2。
根据上述方案及观察到的实验现象回答下列问题:
(1)在操作2中,电流计的指针是否偏转?有无电流产生?试分析原因。
(2)在操作3中,当电流计的两笔头接触两铜丝时,指针是否偏转?有无电流产生?当接触铜丝和铁丝时,指针是否偏转?有无电流产生?试分析原因。
(3)若将操作2中的无水乙醇改为乙酸溶液,观察到的现象相同吗?试分析原因。
(4)该实验说明组成原电池必须具备的条件有:
①_________________________;
②_________________________;
③_________________________。
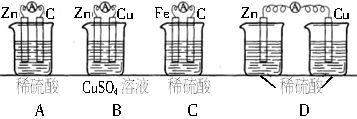
(5)下列装置可以形成原电池的是_____。

(6)根据组成原电池的条件,试以反应Fe+Cu2+=Fe2++Cu设计一个原电池。
供选用的电解质溶液:稀硫酸、硫酸铜溶液、氯化铜溶液。
供选用的电极材料:锌片、铜片、铁片、石墨。
负极材料:______________,电极反应式:________________________________;
正极材料:______________,电极反应式:________________________________;
电解质溶液:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com