
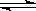 F��(aq) + H2O(l) ��H=��67.7 kJ/mol
F��(aq) + H2O(l) ��H=��67.7 kJ/mol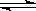 H2O(l) ��H=��57.3kJ/mol
H2O(l) ��H=��57.3kJ/mol| A�����������Һ�¶����ߣ�HF�ĵ���̶ȼ�С�������ǻӷ��� |
B��ˮ������Ȼ�ѧ����ʽΪ��H2O(1) 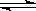 H+(aq)+OH��(aq)����H= +57.3kJ/mol H+(aq)+OH��(aq)����H= +57.3kJ/mol |
| C����c > 0.1ʱ��һ�������ڣ�c(Na+) = c(F��) |
| D������Ϻ���Һ�У�c(Na+)>c(OH��) >c(F��)>c(H+)����cһ��С��0.1 |
 ��ѧ�̸̳����¿α�ϵ�д�
��ѧ�̸̳����¿α�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��CaCO3���������ͳ����ܽⲻ�Ͻ��У���������� |
| B��CaCO3������ˮ���䱥����Һ���������磬�������������Һ |
| C�������¶ȣ�CaCO3�������ܽ������ |
| D����CaCO3�����м��봿����壬CaCO3���ܽ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
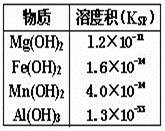
| A��Al3+����ת��ΪAl(OH)3���� |
| B���Ӽ�����У�Fe2+��Mn2+����ͬʱת��Ϊ���� |
| C��ҪʹMg2+ת��Ϊ��������ҺpHӦ����9 |
| D��pH=14ʱ�����ֽ�������ȫ���Գ�����ʽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����AgClˮ��Һ�м������ᣬKspֵ��� |
| B����һ���¶���AgCl��ˮ��Һ�У�Ag+��Cl-���ʵ���Ũ�ȵij˻���һ������ |
C��25oCʱKsp(AgCl)=l��8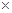 10-10��Ksp(AgI)=1��0��10-16�����AgCl����ת��ΪAgI 10-10��Ksp(AgI)=1��0��10-16�����AgCl����ת��ΪAgI |
| D���¶�һ��ʱ������Һ��Ag+��Cl-���ʵ���Ũ�ȵij˻�����Kspֵʱ������ҺΪAgCl�ı�����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ɫ��NO2�����ѹ����ɫ�ȱ����ٱ�dz |
| B��H2��I2��HI��������ѹ����ɫ���� |
| C����������ת��Ϊ��������ʱ���ӿ�����������߶��������ת���� |
| D������ˮƿ�������д����������ݳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
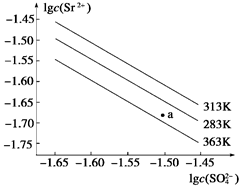
| A���¶�һ��ʱ,Ksp(SrSO4)��c(SO42- )���������С |
| B��������ͬ�¶���,313 KʱKsp(SrSO4)��� |
| C��283 Kʱ,ͼ��a���Ӧ����Һ�DZ�����Һ |
| D��283 K�µ�SrSO4������Һ���µ�363 K���Ϊ��������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢ڢۢܢ� | B���٢ܢۢڢ� | C���ݢܢ٢ڢ� | D���ܢۢݢڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��KspԽ��˵������ʵ��ܽ��Խ�� |
| B��Kspֻ�����ʵı����йأ�������������� |
| C��Ksp��ʾ����ǿ�������ˮ�дﵽ�����ܽ�ƽ��ʱ����Һ������Ũ����֮�� |
| D��Ksp����ֵֻ�����ܵ���ʵ������йأ����¶��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
 PbCO3(s)+SO42��(aq)��ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֡�
PbCO3(s)+SO42��(aq)��ij��������PbSO4Ϊԭ��ģ��ù��̣�̽��������Ӧ��ʵ���������������ijɷ֡�| ʵ�鲽�裨��Ҫ��д������������̣� | Ԥ�ڵ�ʵ������ͽ��� |
| ȡһ������Ʒ��ָ������ | |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com