
���� ��1������Ԫ���л��ϼ۱仯������������ԭ��Ӧ��ʧ�����غ㡢ԭ�Ӹ����غ���ƽ����ʽ��
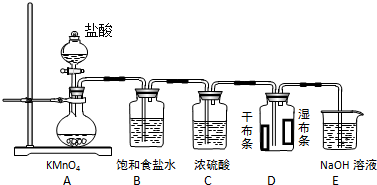
��2�����ݷ���ʽ2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8 H2O��֪������1mol��������2mol�Ȼ�����-1���Ȼ��ϼ����ߣ�ʧȥ2mol���ӣ��ݴ˼���ת��0.5mol���ӣ�������Cl2�����ʵ�����
��3��Ũ���������ˮ�ԣ�
��4������������Ư���ԣ����������Ư���ԣ�
��5���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��6������500mL��Һ��Ӧѡ��500ml����ƿ������m=CVM������Ҫ�������Ƶ�������
��� �⣺��1����Ӧ�и��������+7���̽�Ϊ�Ȼ�����+2�ۣ��Ȼ�����-1���Ȳ�������Ϊ������0�ۣ����ݵ�ʧ�����غ㣬������ϵ��Ϊ5���������ϵ��Ϊ2������ԭ�Ӹ����غ㣬��Ӧ����ʽ��2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8 H2O��
�ʴ�Ϊ��2��16��2��2��5��8��
��2�����ݷ���ʽ2KMnO4+16HCl��Ũ��=2KCl+2MnCl2+5Cl2��+8 H2O��֪������1mol��������2mol�Ȼ�����-1���Ȼ��ϼ����ߣ�ʧȥ2mol���ӣ��ݴ˼���ת��0.5mol���ӣ�������Cl2�����ʵ���0.25mol��
�ʴ�Ϊ��0.25mol��
��3��Ũ���������ˮ�ԣ����Ը���������
�ʴ�Ϊ������������
��4������������Ư���ԣ�������ˮ��Ӧ���ɵĴ��������Ư���ԣ����Կ�������IJ�������ɫ��ʪ��IJ�����ɫ��
�ʴ�Ϊ���ɲ�������ɫ��ʪ������ɫ��
��5���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ�����ӷ���ʽ��Cl2+2OH-=Cl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-=Cl-+ClO-+H2O��
��6������500mL��Һ��Ӧѡ��500ml����ƿ���������NaOH������=0.5mol•L-1��0.5L��40g/mol=10.0g��
�ʴ�Ϊ��500 mL����ƿ��10.0 g��
���� ���⿼����������ʵ�����Ʊ������ʵļ��飬һ�����ʵ���Ũ����Һ�����ƣ���ȷ�������Ʊ�ԭ���������ǽ���ؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ᱵ | B�� | Cu | C�� | NaCl | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
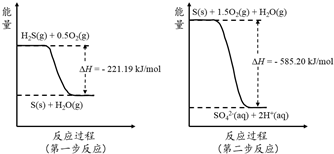
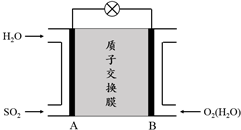
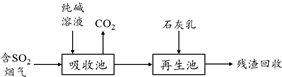
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na2O2+2H2O�T2Na++2OH-+H2�� | B�� | 2O22-+4H+�T4OH-+O2�� | ||
| C�� | Na2O2+2H2O�T2Na++2OH-+O2�� | D�� | 2Na2O2+2H2O�T4Na++4OH-+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
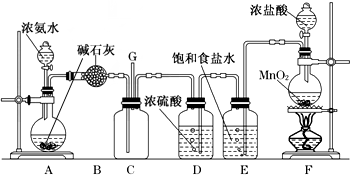
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ����Ȳ | B�� | 1-��ϩ���ױ� | C�� | ���������� | D�� | ���� ��Ȳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
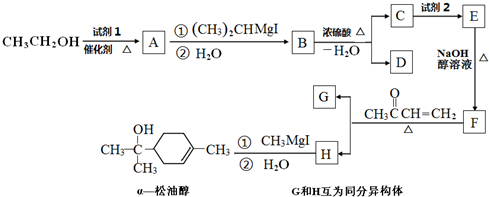
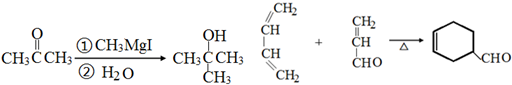
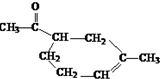 ��
��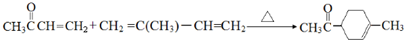 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
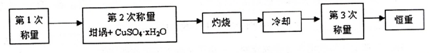

| ����ǰ���� | ���Ⱥ����� | ||
| m1 | m2 | m3 | m4 |
| 11.721g | 22.692g | 18.631g | a |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com