
(1)在①稀硫酸 ②液态HCl ③NaOH溶液 ④蔗糖晶体 ⑤Na3PO4固体⑥铜丝 ⑦液氨 ⑧酒精 ⑨熔融NaCl 上述状态下可导电的是 ;(填写序号,下同) 属于非电解质的是 ; 上述状态下的电解质不能导电的是 。
(2) 写出下列物质的电离方程式:
H2SO4
Ba(OH)2
Na3PO4
(9分)(1)①③⑥⑨; ④⑦⑧; ②⑤
(2) H2SO4==2H++SO42- Ba(OH)2==Ba2++2OH-
Na3PO4==3Na++PO43-
【解析】
试题分析:(1)熔融的离子化合物、电解质溶液、金属均可导电,所以在上述状态下导电的是稀硫酸、氢氧化钠溶液、铜丝、熔融氯化钠,答案选①③⑥⑨;大部分有机物、气态氢化物、非金属氧化物(除H2O外)都是非电解质,所以蔗糖、酒精、液氨都是非电解质,答案选④⑦⑧;液态HCl、Na3PO4固体是电解质,但HCl是共价化合物,熔融下不导电,Na3PO4是离子化合物,但固体不导电,答案选②⑤;
(2)硫酸是强电解质,完全电离产生硫酸根离子和2个氢离子,电离方程式为H2SO4==2H++SO42-;氢氧化钡是强电解质,完全电离产生钡离子和2个氢氧根离子,电离方程式为Ba(OH)2==Ba2++2OH-;磷酸钠是强电解质,完全电离产生磷酸根离子和3个钠离子,电离方程式为Na3PO4==3Na++PO43-。
考点:考查电解质、非电解质、强电解质的判断,电离方程式的书写


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:2014-2015学年江苏省沭阳县高二上学期期中化学试卷(解析版) 题型:实验题
(10分)实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸和浓硝酸的混合酸加入反应器中。
②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。
③在50℃~60℃下发生反应。
④除去混合酸后,粗产品依次用蒸馏水和5%的NaOH溶液洗涤,最后用蒸馏水洗涤。
⑤将用无水氯化钙干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
(1)配制一定比例浓硝酸和浓硫酸混合酸时,操作注意事项是 ;
(2)步骤③的加热方式是 ;
(3)步骤④中,洗涤、分离粗硝基苯应使用的主要玻璃仪器是 ;
(4)步骤④中,粗产品用5%的NaOH溶液洗涤的目的是 ;
(5)纯硝基苯是无色、密度比水 (填“大”或“小”)、具有 气味的油状液体。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省沭阳县高一上学期期中化学试卷(解析版) 题型:选择题
四种基本反应类型与氧化还原反应的关系如下图所示,则下列化学反应属于区域2的是
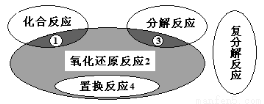
A.Zn + H2SO4 = ZnSO4 + H2↑
B.H2 + Cl2  2HCl
2HCl
C.2KClO3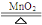 2KCl+3O2↑
2KCl+3O2↑
D.2Cl2+2Ca (OH)2 = CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高一上学期期中化学试卷(解析版) 题型:选择题
对于相同质量的SO2和SO3,下列说法中正确的是
A.硫元素的质量比为5∶4
B.分子数之比为3∶4
C.原子总数之比为3∶4
D.物质的量之比为1∶1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高一上学期10月月考试卷化学试卷(解析版) 题型:填空题
已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验:
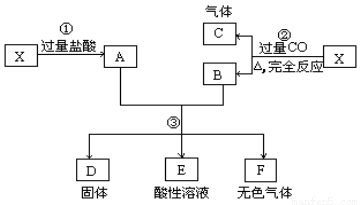
(1)写出①、②和③步所有反应的化学方程式;
; 。
; 。
; 。
(2)设从③步所得固体D的质量为32 g,溶液E中只含有一种金属离子,气体F在标准状况下体积为5.6 L,试计算取用的每份X中FeO与CuO的质量。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高一上学期10月月考试卷化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,32 g O2和O3的混合气体所含原子数为NA
B.标准状况下,1.8g的H2O中含有的电子数为NA
C.常温常压下,11.2L氧气所含的原子数为NA
D.10克氖气所含原子数约为6.02×1023
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高一上学期10月月考试卷化学试卷(解析版) 题型:选择题
下列各组物质中,前者为混合物,后者为单质的是
A.Na2CO3·10H2O 、 Na2CO3 B.盐酸 、 液氮
C.石油 、 冰 D.碘酒 、 干冰
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高一上学期第一次月考化学试卷(解析版) 题型:选择题
取含有 0.02 mol 的硫酸溶液,先投入 0.24 g 镁粉,再滴入NaOH 溶液,当使溶液中的镁离子全部转化为沉淀时, 需要NaOH的物质的量为
A.0.02 mol B.0.03 mol C.0.04 mol D.0.01 mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年度河南省许昌市五校高一上期第一次联考化学试卷(解析版) 题型:填空题
(10分)(1)写出下列物质在水溶液中的电离方程式
氯化铜______________ 硫酸铁______________
(2)下列物质:①Na ② H2O ③酒精 ④CO2 ⑤NH3 ⑥Cu(OH)2 ⑦Ba(OH)2 ⑧冰醋酸(纯净的醋酸) ⑨蔗糖 ⑩NaCl溶液 ?BaSO4。
属于电解质的是 , 属于非电解质的是 。(填序号)
(3)已知浓度为0.01mol·L-1的HCl溶液VmL,加水稀释到2VmL,取出10mL,则这10mL溶液中c(H+) mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com