
【题目】已知一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2↑+9H2O,下列说法正确的是( )
2HNO3+4N2↑+9H2O,下列说法正确的是( )
A. 分解反应都是氧化还原反应B. N2是还原产物,HNO3是氧化产物
C. 被氧化与被还原的氮原子数之比为3∶5D. 每生成4mol N2转移15mol电子
【答案】D
【解析】
在5NH4NO3![]() 2HNO3+4N2↑+9H2O的反应中,铵根离子中的氮元素由-3价升高为0价,被氧化,硝酸根离子中氮元素由+5价降低为0价,被还原,氮气既是还原产物也是氧化产物。
2HNO3+4N2↑+9H2O的反应中,铵根离子中的氮元素由-3价升高为0价,被氧化,硝酸根离子中氮元素由+5价降低为0价,被还原,氮气既是还原产物也是氧化产物。
A.判断一个化学反应是不是氧化还原反应,关键是看有没有元素化合价的变化,如碳酸钙的分解反应CaCO3![]() CaO+CO2↑,因没有元素化合价的变化,就不是氧化还原反应,故A错误;B.根据上述分析可知,氮气既是还原产物也是氧化产物,而由硝酸根离子到硝酸并无元素化合价的变化,所以硝酸既不是氧化产物也不是还原产物,故B错误;C.根据得失电子守恒规律,可知被氧化的氮原子与被还原的氮原子物质的量之比为(5-0):[0-(-3)]=5:3,故C错误;D.根据方程式可知,当生成4mol N2时,有5mol铵根离子失去电子5×[0-(-3)]=15mol,有3mol硝酸根离子得到电子3×(5-0)=15mol,所以每生成4mol N2转移15mol电子,故D正确。答案选D。
CaO+CO2↑,因没有元素化合价的变化,就不是氧化还原反应,故A错误;B.根据上述分析可知,氮气既是还原产物也是氧化产物,而由硝酸根离子到硝酸并无元素化合价的变化,所以硝酸既不是氧化产物也不是还原产物,故B错误;C.根据得失电子守恒规律,可知被氧化的氮原子与被还原的氮原子物质的量之比为(5-0):[0-(-3)]=5:3,故C错误;D.根据方程式可知,当生成4mol N2时,有5mol铵根离子失去电子5×[0-(-3)]=15mol,有3mol硝酸根离子得到电子3×(5-0)=15mol,所以每生成4mol N2转移15mol电子,故D正确。答案选D。


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】把足量熟石灰放入蒸馏水中,一段时间后达到平衡:Ca(OH)2(s)![]() Ca2+(aq)+2OH-(aq),下列叙述正确的是( )
Ca2+(aq)+2OH-(aq),下列叙述正确的是( )
A. 向溶液中加入少量的NaOH固体,则其中的Ca(OH)2的固体增多
B. 向溶液中加入Na2CO3溶液,则其中的Ca(OH)2的固体增多
C. 恒温下向溶液中加入CaO,溶液的pH升高
D. 给溶液加热,溶液的pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4。现将pH和体积都相同的次氯酸和氢氟酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是

A. 曲线I为次氯酸稀释时pH变化曲线
B. 取a点的两种酸溶液,中和相同体积、相同浓度的NaOH溶液,消耗次氯酸的体积较小
C. a点时,若都加入相同大小的锌粒,此时与氢氟酸反应的速率大
D. b点溶液中水的电离程度比c点溶液中水的电离程度小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、CH3OH既是重要的化工原料,又是未来重要的能源物质。
(1)将1.0 mol CH4和2.0 mol H2O(g) 通入容积为2L的反应室,在一定条件下发生反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
(2)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g) ![]() CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
a.恒容条件下充入He b.增大体积
c.升高温度 d.投入更多的H2O(g)
(3)在恒容条件下进行反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
a.消耗1 mol CO2同时生成1 mol CH3OH b.容器内压强保持不变
c.混合气体的密度保持不变 d.CH3OH(g)的浓度保持不变
(4)以KOH为电解质的甲醇-空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图。 回答下列问题:

①该原电池的正极是____(填“甲”或“乙”),电解过程中乙电极附近pH____(填“增大”或“减小”);
②负极的电极反应式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式氯化铜[CuaClb(OH)c·xH2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。步骤1:将铜粉加入稀盐酸中,并持续通空气反应生成CuCl2。已知Fe3+对该反应有催化作用,其催化原理如下图所示。步骤2:在制得的CuCl2溶液中,加入石灰乳充分反应后即可制备碱式氯化铜。
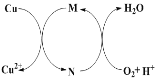
下列有关说法正确的是
A. a、b、c 之间的关系式为:a=b+c
B. 图中M、N分别为Fe2+、Fe3+
C. 步骤1充分反应后,加入少量CuO是为了除去Fe3+
D. 若制备1 mol的CuCl2,理论上消耗11.2 LO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由20g两种金属粉末组成的混合物,与足量的盐酸反应后得到标准状况下11.2L氢气,这种金属混合物的组成可能是( )
A. Mg和AlB. Fe和ZnC. Al和FeD. Zn和Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是重要的基本化工原料,广泛用于化学、冶金、造纸、纺织、医药、石油等工业,以及饮用水消毒、污水处理等方面。
(1)实验室制取Cl2的反应方程式为:4HCl(浓)+MnO2![]() Cl2↑+MnCl2+2H2O。该反应中氧化剂和还原剂物质的量之比为_________;
Cl2↑+MnCl2+2H2O。该反应中氧化剂和还原剂物质的量之比为_________;
(2)KMnO4和盐酸反应也可制取Cl2:
____KMnO4+____HCl=____KCl+____MnCl2+____Cl2↑+____H2O
请配平该反应方程式。当标准状况下有11.2L氯气生成时,该反应转移电子的数目为_____。
(3)用氯氧化法可处理含KCN的废水。液氯在碱性条件下可以将氰化物氧化成毒性仅为氰化物的千分之一的氰酸盐,氰酸盐再进一步被氧化为无毒物质。
①由反应KCN+2KOH+Cl2 = KOCN + 2KCl+H2O判断,氰酸盐KOCN中C元素的化合价为_________(已知反应前后氮元素化合价未改变);
②投入过量液氯,可将氰酸盐进一步氧化为氮气。请用单线桥法标出电子转移的方向和数目:
2KOCN+4KOH+ 3Cl2 = 2CO2↑ + N2 ↑+6KCl + 2H2O
______________________________
③若某厂废水中含KCN的浓度为0.65g/L,处理上述废水20.0 L,使KCN完全转化为无毒物质,至少需液氯的物质的量为___________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)6.02×1023个氢氧根离子的物质的量是________mol,其摩尔质量为________。
(2)在标准状况下,0.01 mol某气体的质量为0.44 g,则该气体的密度为________g·L1(保留小数点后两位),该气体的相对分子质量为________。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是________,CO的体积分数是________,CO的质量分数是________,C和O原子个数比是________,混合气体的平均相对分子质量是________,密度是________g·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示为海水综合利用的部分流程,下列有关说法正确的是
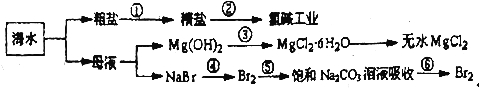
A. 第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质加入的药品顺序为NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B. 第②步是一个将电能转化为化学能的过程,工业上可采用石墨为电极,采用阴离子交换膜的电解装置
C. 第③步中结晶出的MgC12·6H2O可在空气中受热分解制无水MgC12
D. 第④步中反应的离子方程式为C12+2Br-=2C1-+Br2,第④⑤步的目的是富集溴元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com