
【题目】下列关于氯气及其化合物的叙述不正确的是
A. 新制氯水久置后酸性增强
B. 因为氯气有毒,所以可用于杀菌,消毒,漂白
C. 除去氯气中少量氯化氢可使气体通过饱和食盐水
D. 新制备的氯水可使蓝色石蕊试液先变红后褪色
科目:高中化学 来源: 题型:
【题目】将![]() 明矾溶于水形成100mL溶液,以下说法正确的是
明矾溶于水形成100mL溶液,以下说法正确的是![]()
A. 明矾净水是利用了明矾的强氧化性
B. 溶液的焰色反应为紫色,这是化学性质
C. 加入![]() 溶液至沉淀物质的量达到最大,消耗
溶液至沉淀物质的量达到最大,消耗![]() 溶液
溶液![]()
D. 加入![]() 溶液至
溶液至![]() 恰好完全沉淀,
恰好完全沉淀, ![]() 全部转化为
全部转化为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳族元素包括碳、硅、锗(Ge)、锡(Sn)、铅等,它们的单质及化合物广泛应用于我们生活的各个领域。锗和锡以前曾被用于半导体材料,铅被用来制造蓄电池。碳族元素在化合物中只有铅以低价形式存在时较稳定,其它元素在化合物中都是以高价形式存在比较稳定,回答下列问题:
Ⅰ.(1)高岭土的成分中含Al2(Si2O5)(OH)4,请改写成氧化物的形式_________________;
(2)实验室用单质锡粉制取少量二氯化锡溶液,制取和保存的方法是(用文字叙述)___________________;
(3)铅有多种氧化物,写出四氧化三铅与浓盐酸反应的离子方程式_____________________;二氧化铅在空气中强热会得到一系列铅的其它氧化物。若把239g二氧化铅强热,当质量变为231g时,写出反应的化学方程式____________________________。
Ⅱ.CH4–CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
CH4–CO2催化重整反应为:CH4(g)+ CO2(g)![]() 2CO(g)+2H2(g)。
2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4 (g) ΔH=–75 kJ·mol1 ①C(s)+O2(g)=CO2(g) ΔH=–394 kJ·mol1②2C(s)+O2 (g)=2CO(g) ΔH=–222kJ·mol1③
(1)有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
(2)若该反应在容积不变的绝热容器中进行,能够判断该反应已达到平衡的是____(填标号)。
A、c(CO2)/c(H2)不再发生变化 B.气体的密度不再发生变化 C.气体的平均摩尔质量不再发生变化 D.每有8molC-H键生成的同时有4molH-H键的断裂 E.容器的温度不再发生变化
(3)T℃时,在体积为10 L的容器中加入10 mol CH4、5 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,此温度下,该反应的化学平衡常数K=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示对应化学反应的离子方程式正确的是
A. 碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++H2O+CO2↑
B. 铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
C. 向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓
D. 用银氨溶液检验乙醛中的醛基:CH3CHO+[Ag(NH3)2]++2OH- ![]() CH3COO-+NH4++NH3+ Ag↓+H2O
CH3COO-+NH4++NH3+ Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| 选项 | a | b | c |
A | Al | AlCl3 | Al(OH)3 | |
B | CO2 | Na2CO3 | NaHCO3 | |
C | Si | SiO2 | H2SiO3 | |
D | S | SO3 | H2SO4 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】双酚A是食品、饮料包装和奶瓶等塑料制品的添加剂,能导致人体内分泌失调,对儿童的健康危害更大。下列有关双酚A的叙述不正确的是( )
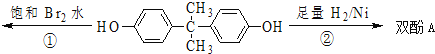
A. 双酚A能与碳酸钠溶液反应,能与FeCl3溶液发生显色反应
B. 双酚A的核磁共振氢谱显示氢原子数之比是1∶2∶2∶3
C. 反应①中,1mol双酚A最多消耗4molBr2
D. 反应②的产物与足量钠反应放出1molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为 M 的气态化合物V L(标准状况),溶于m g 水中,得到质量分数为 w、物质的量浓度为c mol/L、密度为ρg/mL 的溶液,下列说法正确的是
A. 溶液密度ρ=cw/1000M B. 物质的量浓度c=ρV/(MV+22.4m)
C. 溶液的质量分数w=MV/22.4m D. 对分子质量M=22.4mw/(1—w)V
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A.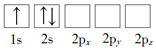 B.
B.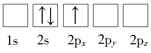
C.![]() D.
D.![]()
(2)Li+与H具有相同的电子构型,r(Li+)小于r(H),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图(a)的BornHaber循环计算得到。
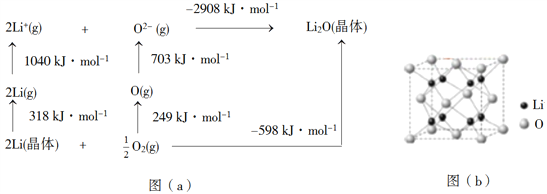
可知,Li原子的第一电离能为________kJ·mol1,O=O键键能为______kJ·mol1,Li2O晶格能为______kJ·mol1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com