
【题目】CN-可以造成水体污染,某小组采用如下方法对污水进行处理。
Ⅰ![]() 双氧水氧化法除NaCN。
双氧水氧化法除NaCN。
(1)NaCN的电子式为____________________________。
(2)碱性条件下加入双氧水除CN-,可得到纯碱和一种无色无味的无毒气体,该反应的离子方程式为________________。
Ⅱ.CN-和Cr2O72-联合废水处理法。
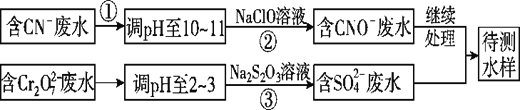
(3)②中反应后无气体放出,该反应的离子方程式为_____________________。
(4)步骤③中,每处理0.4mol Cr2O72-,至少消耗Na2S2O3________mol。
【答案】![]() 5H2O2+2CN-+2OH-=N2↑+2CO32-+6H2OCN-+ClO-=CNO-+Cl-0.3mol
5H2O2+2CN-+2OH-=N2↑+2CO32-+6H2OCN-+ClO-=CNO-+Cl-0.3mol
【解析】
(1)NaCN为离子化合物,CN-中各原子均满足8电子稳定结构,存在C≡N键,电子式为![]() ;
;
(2)碱性条件下加入双氧水除CN-,可得到纯碱和一种无色无味的无毒气体,碱性气体为氨气,氰化钠溶液的CN-被双氧水氧化为CO32-,同时放出NH3,反应的化学方程式为5H2O2+2CN-+2OH-=N2↑+2CO32-+6H2O;
(3)步骤②中无气体放出,CN-被ClO-氧化为CNO-,又因为是在碱性环境中,故ClO-只能被还原为Cl-,反应式为CN-+ClO-=CNO-+Cl-;
(4)步骤③的离子反应为3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O,因此每处理0.4mol Cr2O72-,消耗Na2S2O3的物质的量是0.3mol。


科目:高中化学 来源: 题型:
【题目】相同浓度的NaCl、MgCl2、AlCl3溶液,分别与AgNO3溶液反应,当生成的AgCl沉淀的质量之比为3:2:1时,三种溶液的体积比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X的结构如下,下列有关X的说法正确的是( )
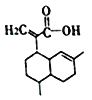
A. X的分子式为C15H24O2
B. 1molX最多可以和3molH2发生加成反应
C. X能发生取代反应和加成反应
D. X可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且褪色原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如右图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )
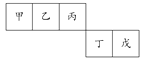
A. 最外层电子数:甲>乙>丙>丁>戊
B. 简单离子的离子半径:戊>丁
C. 含有丁元素的酸有多种
D. 乙的氢化物多种多样,丙、丁、戊的氢化物各有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验室产生的废液中含有大量会污染环境的物质,为了保护环境,这些废液必须经处理后才能排放。某化学实验室产生的废液中含有两种金属离子:Fe3+、Cu2+,化学小组设计了如下图所示的方案对废液进行处理,以回收金属,保护环境。
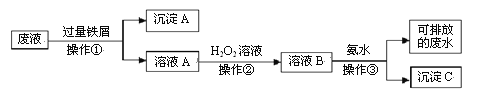
(1)操作①的名称是_____。
(2)沉淀A中含有的金属单质有__________。
(3)操作②中观察到的实验现象是_____________。
(4)检验溶液B中含有的金属阳离子常用的试剂是___________。
(5)操作③中发生反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
A、B、D、E、F为原子序数依次增大的前四周期元素,其中A的最外层电子数是其内层电子数的2倍,B、D、E为同周期元素,B原子的核外电子总数是其未成对电子数的5倍,E原子最外层有1个未成对电子,F原子核外有22种运动状态的电子。请回答下列问题:
(1)F元素位于周期表___________区,其价电子排布图为:___________。
(2)B、D、E三种元素中,第一电离能最小的是_______________________ (填元素符号);写出AD2的等电子体___________ (分子和阴离子各写一种)。
(3)AO2和DO2熔点高的是___________,原因是___________。
(4)B的单质和E的单质反应可形成原子个数比为1∶3的化合物M,M的立体构型为___________,中心原子的杂化轨道类型为___________。
(5)元素F有两种同素异形体,常温下是六方堆积,高温下是体心立方堆积。如图所示是F晶体的一种晶胞,晶胞参数a=0.295nm,c=0.469nm,则该F晶体的密度为___________g·cm-3(用NA表示阿伏加德罗常数的值,列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了使Na2S溶液中c(Na+)/c(S2-)的比值变小,可采取的措施是( )
①适量盐酸 ②适量NaOH(s) ③适量KOH(s) ④适量KHS(s) ⑤加水 ⑥适量Cl2溶液⑦加热
A. ②③④ B. ①②⑤⑥⑦
C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】米饭遇到碘酒时显蓝色,咀嚼米饭后有甜味,这说明( )
A. 米饭中只含有淀粉 B. 米饭咀嚼后只含单糖
C. 米饭咀嚼时单糖聚合成淀粉 D. 米饭咀嚼时淀粉发生了水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R 代表)。回答下列问题:
(1)基态N 原子中,核外电子占据的最高能层的符号是______________,占据该能层电子的电子云轮廓图形状为_______________________________。
(2)N 和O 两种元素第一电离能大小关系是N__________( 填“ >”“ <” 或“ =” )O,其原因是____________;N 和O两种元素电负性大小关系是N_______(填“ >”“ <” 或“=” )O。
(3)经X-射线衍射测得化合物R 的晶体结构,其局部结构如下图所示。

①组成化合物R 的两种阳离子中σ键的个数之比为_________;其中四核阳离子的立体构型为___________,其中心原子的杂化轨道类型是_______________________。
②分子中的大π键可用符号![]() 表示,其中m 代表参与形成的大π键原子数,n 代表参与形成的大π键电子数,如苯分了中的大π键可表示为
表示,其中m 代表参与形成的大π键原子数,n 代表参与形成的大π键电子数,如苯分了中的大π键可表示为![]() 。则N5-中的大π键应表示为___________________。
。则N5-中的大π键应表示为___________________。
③氢键通常用X-H…···Y 表示,请表示出上图中的所有氧键:_________________。
④R的立方晶胞参数为a nm,晶胞中含有Y个(N5)6(H3O)3(NH4)4Cl 单元,如果(N5)6(H3O)3(NH4)4Cl的相对分子质量用M 表示,阿伏加德罗常数的值为NA,则R 晶体的密度为________g·cm-3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com