
已知:2 CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol根据以上热化学方程式判断,下列说法错误的是
| A.CO2气体分解生成CO气和O2气体的反应是放热反应 |
| B.CO气体与O2气体生成CO2气体的反应是放热反应 |
| C.上图可表示由CO气体生成CO2气体的反应过程和能量关系 |
| D.在相同条件下,2 mol CO气体与1 mol O2气体的能量总和大于2 mol CO2气体的能量 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2011-2012年呼伦贝尔市牙克石林业一中高一下学期期末考试化学试卷(带解析) 题型:填空题
(6分).2CO(g)+O2(g) 2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题:
2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题: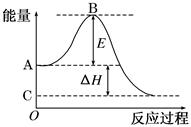
(1)图中A点表示:____________________________________;E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH = ________kJ/mol。
查看答案和解析>>
科目:高中化学 来源:2014届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知:2 CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol根据以上热化学方程式判断,下列说法错误的是
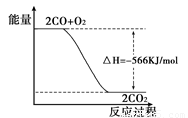
A.CO2气体分解生成CO气和O2气体的反应是放热反应
B.CO气体与O2气体生成CO2气体的反应是放热反应
C.上图可表示由CO气体生成CO2气体的反应过程和能量关系
D.在相同条件下,2 mol CO气体与1 mol O2气体的能量总和大于2 mol CO2气体的能量
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
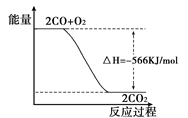
已知:2 CO(g) + O2(g) = 2CO2(g) △H=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802kJ/mol
H2O(g)= H2O(l) △H=-44KJ/mol
则CH4在空气中不完全燃烧时,热化学方程式是
A.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) △H=-1038kJ/mol
B.4CH4(g)+7O2(g)=2CO2(g)+2CO(g)+8H2O(l) △H=-2642kJ/mol
C.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) △H=-1497kJ/mol
D.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(l) △H=-1497kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com