
��֪��2 CO(g)��O2(g)===2CO2(g) ��H����566 kJ/mol���������Ȼ�ѧ����ʽ�жϣ�����˵���������
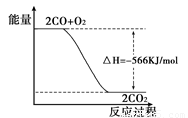
A��CO2����ֽ�����CO����O2����ķ�Ӧ�Ƿ��ȷ�Ӧ
B��CO������O2��������CO2����ķ�Ӧ�Ƿ��ȷ�Ӧ
C����ͼ�ɱ�ʾ��CO��������CO2����ķ�Ӧ���̺�������ϵ
D������ͬ�����£�2 mol CO������1 mol O2����������ܺʹ���2 mol CO2���������
A
��������
���������2 CO(g)��O2(g)===2CO2(g) ��H����566 kJ/mol��һ����̼��ȼ���Ƿ��ȷ�Ӧ������CO2����ֽ�����CO����O2����ķ�Ӧ�����ȷ�Ӧ����A����Ϊ����Ĵ𰸣�CO������O2��������CO2����ķ�Ӧ�Ƿ��ȷ�Ӧ����B��ȷ��CO������O2��������CO2����ķ�Ӧ�Ƿ��ȷ�Ӧ�����Է�Ӧ��������������������������������ͼ�ɱ�ʾ��CO��������CO2����ķ�Ӧ���̺�������ϵ����CD��ȷ��
���㣺��ѧ��Ӧ�����ı仯
���������⿼���˻�ѧ��Ӧ�����ı仯���ÿ����Ǹ߿������Ŀ��㣬����Ҫ����ö���һ�����ȷ�Ӧ����Ӧ��������������������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ���ѡ��
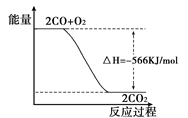
��֪��2 CO(g)��O2(g)===2CO2(g) ��H����566 kJ/mol���������Ȼ�ѧ����ʽ�жϣ�����˵���������
| A��CO2����ֽ�����CO����O2����ķ�Ӧ�Ƿ��ȷ�Ӧ |
| B��CO������O2��������CO2����ķ�Ӧ�Ƿ��ȷ�Ӧ |
| C����ͼ�ɱ�ʾ��CO��������CO2����ķ�Ӧ���̺�������ϵ |
| D������ͬ�����£�2 mol CO������1 mol O2����������ܺʹ���2 mol CO2��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012����ױ���������ʯ��ҵһ�и�һ��ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ������
��6�֣���2CO(g)��O2(g) 2CO2(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol CO (g)����Ϊ1 mol CO2 (g)�Ħ�H ����283 kJ/mol����ش��������⣺
2CO2(g)��Ӧ���̵������仯��ͼ��ʾ����֪1 mol CO (g)����Ϊ1 mol CO2 (g)�Ħ�H ����283 kJ/mol����ش��������⣺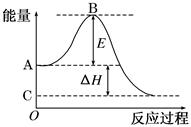
(1)ͼ��A���ʾ��____________________________________��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ��________(��С����ޡ�)Ӱ�졣
(2)ͼ�Ц�H �� ________kJ/mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��2 CO(g) + O2(g) = 2CO2(g) ��H=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ��H=-802kJ/mol
H2O(g)= H2O(l) ��H=-44KJ/mol
��CH4�ڿ����в���ȫȼ��ʱ���Ȼ�ѧ����ʽ��
A��2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) ��H=-1038kJ/mol
B��4CH4(g)+7O2(g)=2CO2(g)+2CO(g)+8H2O(l) ��H=-2642kJ/mol
C��2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) ��H=-1497kJ/mol
D��2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(l) ��H=-1497kJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com