


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I、Ⅱ两途径最终达到平衡时,体系内混合气的百分组成相同 | ||
| B、I、Ⅱ两途径最终达到平衡时,体系内混合气的平均相对分子质量相同 | ||
| C、达平衡时,I途径的反应速率vA等于Ⅱ途径的反应速率vA | ||
D、达平衡时,I途径所得混合气的密度为Ⅱ途径所得混合气密度的
|
查看答案和解析>>
科目:高中化学 来源: 题型:
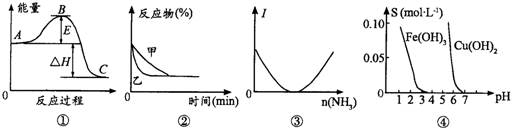
| A、根据图①判断,物质A反应生成物质C的△H>0 | B、压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响可用图②表示 | C、往乙酸溶液中通入氨气至过量,溶液导电能力(I)的变化可用图③表示 | D、根据图④溶解度(s)与溶液pH的关系,若要除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH至4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com