
分析 (1)氢氧化钡为强电解质,完全电离;
(2)硝酸与碳酸氢钠反应生成硝酸钠和二氧化碳、水;
(3)氧化铝为两性物质既能与强酸又能与强碱反应生成盐和水;
硝酸与强酸不反应;
碳酸氢钠与强酸反应生成盐和二氧化碳和水;与强碱反应生成碳酸盐和水;
氢氧化钡与强碱不反应.
解答 解:(1)氢氧化钡为强电解质,完全电离,电离方程式:Ba(OH)2═Ba2++2OH-;
故答案为:Ba(OH)2═Ba2++2OH-;
(2)硝酸与碳酸氢钠反应生成硝酸钠和二氧化碳、水,离子方程式:H++HCO3-═H2O+CO2↑;
故答案为:H++HCO3-═H2O+CO2↑;
(3)氧化铝为两性物质既能与强酸又能与强碱反应生成盐和水;
硝酸与强酸不反应;
碳酸氢钠与强酸反应生成盐和二氧化碳和水;与强碱反应生成碳酸盐和水;
氢氧化钡与强碱不反应;
所以既能与强酸反应,又能与强碱反应的物质是①③;
故答案为:①③.
点评 本题考查了电解质电离方程式书写、离子方程式的书写、元素化合物性质,明确反应实质及物质的性质是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:多选题
| A. | 取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中一定含有结晶水 | |
| B. | 取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴KSCN溶液,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量样品溶于水,滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量样品放入试管中,加入少量浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
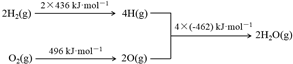
| A. | 1molC(s)完全燃烧放出110 kJ的热量 | |
| B. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-480 kJ•mol-1 | |
| C. | C(s)+H2O(g)═CO(g)+H2(g)△H=+130 kJ•mol-1 | |
| D. | 欲分解2 mol H2O(l),至少需要提供4×462 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用前检查是否漏水 | B. | 溶液未冷却即注入容量瓶中 | ||
| C. | 容量瓶可长期存放溶液 | D. | 在容量瓶中直接溶解固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、SO42-、HCO3- | B. | Na+、Ba2+、Cl-、SO42- | ||
| C. | Cu2+、Ca2+、Cl-、NO3- | D. | Fe2+、K+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 实验操作 | 实验现象 |
| 甲 | ①取少量粉末,加入过量浓硝酸 ②向上述溶液中加入几滴NaCl溶液 | 粉末溶解,有红棕色气体产生 有白色沉淀生成 |
| 乙 | ③取少量粉末,加入足量NaOH溶液 ④向上述溶液中逐滴加入稀盐酸 ⑤继续加入过量的稀盐酸 | 粉末溶解,有气泡产生 有白色沉淀生成 白色沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂混合不一定发生氧化还原反应 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加且有单质生成的反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
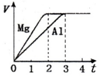 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系| A. | 物质的量之比为3:2 | B. | 质量之比为2:3 | ||
| C. | 摩尔质量之比为2:3 | D. | 反应速率之比为3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com