
| A�� | Fe3O4������ϡ HNO3 ��Ӧ��Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| B�� | ��С�մ�����θ����ࣺNaHCO3+H+=Na++CO2��+H2O | |
| C�� | ˫��ˮ�м���ϡ����� KI ��Һ��H2O2+2H++2I-=I2+2H2O | |
| D�� | ��̼�������Һ�е�����������������Һ��Ca2++2OH-+2HCO3-=CaCO3��+2H2O+CO32- |
���� A������������ԭ��Ӧ������������NO��ˮ��
B��С�մ���ˮ����ȫ���룻
C������������ԭ��Ӧ����ѭ���ӡ�����غ㣻
D����Ӧ����̼��ơ�ˮ��NaOH��
��� �⣺A��Fe3O4������ϡ HNO3 ��Ӧ�����ӷ�ӦΪ3Fe3O4+NO3-+28H+=9Fe3++NO��+14H2O����A����
B����С�մ�����θ���������ӷ�ӦΪHCO3-+H+=CO2��+H2O����B����
C��˫��ˮ�м���ϡ����� KI ��Һ�����ӷ�ӦΪH2O2+2H++2I-=I2+2H2O����C��ȷ��
D����̼�������Һ�е�����������������Һ�����ӷ�ӦΪCa2++OH-+HCO3-=CaCO3��+H2O����D����
��ѡC��
���� ���⿼�����ӷ�Ӧ����ʽ����д��Ϊ��Ƶ���㣬���շ����ķ�Ӧ�����ӷ�Ӧ����д����Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע�����ӷ�Ӧ�б�����ѧʽ�����ʼ����ӡ�����غ㣬��Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ��ʯ���ڴ��CaCO3+2H+�TCa2++CO2��+H2O | |
| B�� | Na2C03��Һ�Լ��ԣ�C032-+H2O�THCO3-+OH- | |
| C�� | ������м����ϡ���Fe+4H++NO3-�TFe3++NO��+2H2O | |
| D�� | FeI2��Һ��ͨ������������2Fe2++C12�T2Fe3++2Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ع���ʱ�������ɸ���ͨ�����·�������� | |
| B�� | ��״���£���Ӧ3.36L������ת�Ƶ���0.2mol | |
| C�� | ����ȼ�ϵ�����������ʲ���ͬ������ֱ��ȼ�յ����������� | |
| D�� | ����Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
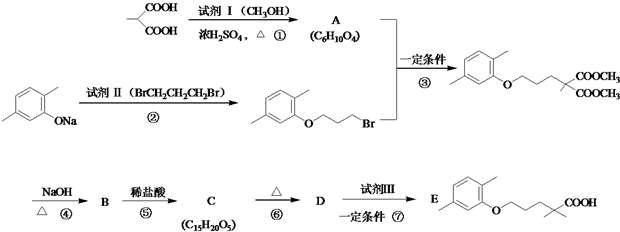
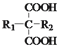 $\stackrel{��}{��}$
$\stackrel{��}{��}$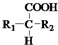 +CO2����R1��R2���������
+CO2����R1��R2���������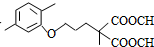 $\stackrel{��}{��}$
$\stackrel{��}{��}$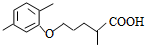 +CO2����
+CO2����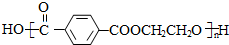 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���շϾɵ�أ���ҪĿ���ǻ������еĹ���� | |
| B�� | ����ʯ��ʹ�ã����÷��ܡ�̫���ܡ�ȼú����Դ��������ɫ��ѧ������ | |
| C�� | ��ʳƷ���з���ʢ�й轺����С�����ɷ�ֹʳ���������� | |
| D�� | �ý��ݹ����������Һ�Ĺ���������ˮ���е���ϩ������ʵ��ˮ�����ʵ�Ŀ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
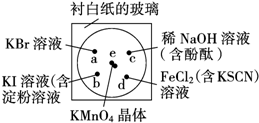 ��ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol/L ��KBr��KI����������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ���ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O��
��ѧʵ����ͻ�����Ч�ؼ�����Ⱦ��ʵ�ֻ�ѧʵ����ɫ����Ҫ��ijѧ�������в�����һ��ʵ�飺��һ���³İ�ֽ�IJ���Ƭ�IJ�ͬλ�÷ֱ�μ�Ũ��Ϊ0.1mol/L ��KBr��KI����������Һ����NaOH������̪����FeCl2����KSCN����Һ��1�Σ�ÿ��Һ�α˴˷ֿ���Χ�ɰ뾶С�ڱ������Բ�Σ���ͼ��ʾ������Բ�Ĵ�����2��֥������С��KMnO4���壬��KMnO4����μ�һ��Ũ���ᣬ��������������Ǻã�����֪��2KMnO4+16HCl��Ũ���T2KCl+2MnCl2+5Cl2��+8H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.1 mol•L-1�Ĵ�����Һ�м�ˮ��ͨ��HCl���嶼��ʹ$\frac{c��{H}^{+}��}{c��C{H}_{3}COOH��}$ֵ���� | |
| B�� | 0.1 mol•L-1�Ĵ�������Һ20 mL��0.1 mol•L-1����10 mL��Ϻ���Һ�����ԣ�����c��CH3COO-����c��Cl-����c��H+����c��CH3COOH�� | |
| C�� | �����ʵ���Ũ�ȵ������NH4HSO4��NaOH��Һ��ϣ�c ��Na+���Tc ��SO42-����c��NH4+����c��H+����c��OH-�� | |
| D�� | 0.1 mol•L-1ijһԪ��HA��Һ��$\frac{c��O{H}^{-}��}{c��{H}^{+}��}$=1��10-8�������Һ����ˮ�������c��H+��=1��10-11mol•L-1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com