
【题目】将X气体通入BaCl2溶液,未见沉淀生成,然后通入Y气体,有沉淀生成,X、Y不可能是( )
A.SO2、H2SB.Cl2、CO2
C.NH3、CO2D.SO2、Cl2
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. K2FeO4可代替Cl2处理饮用水,有杀菌消毒作用
B. CaO2属于碱性氧化物,也属于离子化合物,其阴阳离子个数比为1:2
C. 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了保鲜水果
D. 高温下可用金属钠还原四氯化钛来制取金属钛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下:
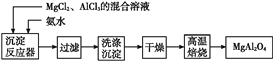
(1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为_____________。
(2)判断流程中沉淀是否洗净所用的试剂是__________________。
(3)在25 ℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式:_____________。{已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34}。
(4)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
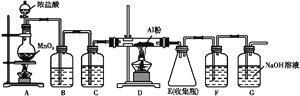
装置B中盛放饱和NaCl溶液,该装置的主要作用是______;F中试剂的作用是__________________________________________。
(5)将Mg、Cu组成的3.92 g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792 L(标准状况),向反应后的溶液中加入4 mol·L-1的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的短周期元素,已知A、B、D三种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4。
(1)写出下列元素符号: B________,D________。
(2)A与D两元素可形成化合物,用电子式表示其化合物的形成过程:________。
(3)A在空气中燃烧生成原子个数比为1:1的化合物,写出其电子式为________。
(4)元素C的最高价氧化物与元素A的最高价氧化物的水化物反应的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取0.55mol/L的NaOH溶液50mL与0.25mol/L的硫酸50mL置于下图所示的装置中进行中和热的测定实验。回答下列问题:

(1)从图中实验装置看,其中尚缺少的一种玻璃用品是______________,除此之外,装置中的一个明显错误是_____________________________。
(2)为保证该实验成功该同学采取了许多措施,如图的碎泡沫塑料的作用在于____________________________________。
(3)实验数据如下表:
①请填写下表中的空白:
温度 实验序号 | 起始温度t1(℃) | 终止温度t2(℃) | 温度差平均值 (t2-t1)(℃) | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.5 | ___________ |
2 | 27.0 | 27.4 | 27.2 | 32.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.2 | |
4 | 26.4 | 26.2 | 26.3 | 29.8 | |
②近似认为实验所用溶液的密度都是1 g/cm3,中和后溶液的比热容c=4.18 J/(g·℃)。根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式(计算结果保留一位小数):_______________。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)________。
a.实验装置保温、隔热效果差
b.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
(4)如果用含0.5mol Ba(OH)2的稀溶液与足量稀硫酸溶液反应,反应放出的热____57.3 kJ(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象 _____________。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式_____________。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)
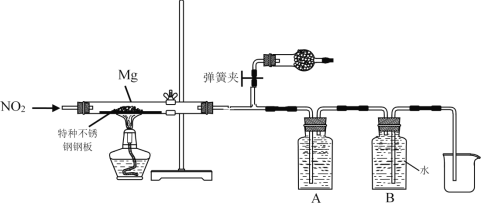
资料信息:2NO2 + 2NaOH = NaNO3 + NaNO2 + H2O
①装置A中的试剂是_____________。
②干燥管和装置B的作用分别是_____________、_____________。
③实验开始时正确的操作步骤是_____________。
a.通入NO2 b.打开弹簧夹
c.点燃酒精灯 d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
(4)实验结束时,同学们观察到与预测相符合的现象,但当用水洗涤硬质玻璃管时,固体遇水产生有刺激性气味的气体,该气体能使湿润的石蕊试纸变蓝。
①同学们认为硬质玻璃管中还发生了另一个反应,该反应为_____________,
②请用化学方程式解释加水产生该气体的原因_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g) △H<0,在恒容的密闭容器中,下列有关说法正确的是
2N2(g)+3H2O(g) △H<0,在恒容的密闭容器中,下列有关说法正确的是
A. 平衡时,其他条件不变,升高温度可使该反应的速率加快,平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1∶2时 ,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com