
【题目】现有等体积混合而成的4组气体.①NO2+NO、②NO2+O2、③HCl+N2、④Cl2+SO2 . 现将其分别通入体积相同的试管中并立即倒立在足量水中,试管内水面上升的高 度分别为h1、h2、h3、h4 , 则高度关系是( )
A.h4>h2>h3>h1
B.h4>h3>h2>h1
C.h2>h3>h1>h4
D.h3>h2>h1>h4
【答案】A
【解析】解:①二氧化氮和水能反应生成硝酸和一氧化氮3NO2+H2O=2HNO3+NO,一氧化氮和水不反应,根据方程式知,气体减少的体积是二氧化氮的 ![]() ,二氧化氮占混合气体的
,二氧化氮占混合气体的 ![]() ,所以试管内气体减少的体积为试管体积的
,所以试管内气体减少的体积为试管体积的 ![]() ,故水面上升的高度为试管的
,故水面上升的高度为试管的 ![]() ;
;
②二氧化氮和氧气、水能反应生成硝酸4NO2+O2+2H2O=4HNO3 , 根据方程式知,氧气剩余,参加反应的氧气的体积为氧气总体积的 ![]() ,二氧化氮全部参加反应,所以混合气体减少的体积为试管体积的
,二氧化氮全部参加反应,所以混合气体减少的体积为试管体积的 ![]() ,故水面上升的高度为试管的
,故水面上升的高度为试管的 ![]() ;
;
③氯化氢极易溶于水,氮气和水不反应,所以混合气体减少的体积为试管体积的 ![]() ,故水面上升的高度为试管的
,故水面上升的高度为试管的 ![]() ;
;
④氯气和二氧化硫、水能发生氧化还原反应生成氯化氢和硫酸Cl2+SO2+2H2O=2HCl+H2SO4 , 且这两种物质极易溶于水,根据方程式知,这两种物质完全反应,没有气体剩余,所以水充满整只试管.
故选A.
【考点精析】掌握氯气的化学性质是解答本题的根本,需要知道氯气的化学性质:与金属反应将金属氧化成高价态;非金属反应;与水反应;与碱反应;与还原性物质反应.


科目:高中化学 来源: 题型:
【题目】对下列实验现象的解释不正确的是
选项 | 实验现象 | 解释 |
A | C12使鲜艳的红色花瓣褪色 | Cl2具有强还原性 |
B | NH3与HCl气体接触时有白烟产生 | NH3与HCl反应生成固体小颗粒 |
C | 新切开的Na表面在空气中很快变暗 | Na容易与空气中的氧气等反应 |
D | 氯化铝溶液中滴入过量的氢氧化钠溶液,白色沉淀溶解 | 氢氧化铝具有两性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学做了如下实验:
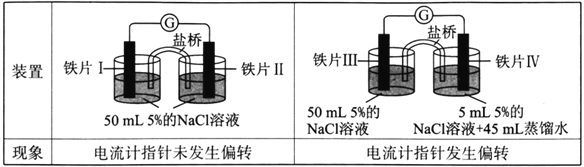
下列说法中正确的是
A. 加热铁片I所在烧杯,电流表指针会发生偏转
B. 用KSCN溶液检验铁片Ⅲ、IV附近溶液,可判断电池的正、负极
C. 铁片I、Ⅲ的腐蚀速率相等
D. “电流计指针未发生偏转”,说明铁片I、铁片Ⅱ均未被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答问题:
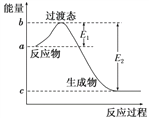
(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。
(2)0.1 mol Cl2与焦炭、TiO2完全反应,生成一种还原性气体和一种易水解成TiO2·xH2O的液态化合物,放热4.28 kJ,该反应的热化学方程式为__________。
(3)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH=+49.0 kJ·mol-1
②CH3OH(g)+![]() O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)===CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸气燃烧为液态水的热化学方程式为____________________________________________________________________。
(4)在微生物作用的条件下,NH经过两步反应被氧化成NO。这两步的能量变化如图:
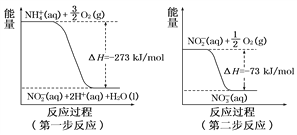
第二步反应是__________反应(填“放热”或“吸热”)。1 mol NH(aq)全部氧化成NO(aq)的热化学方程式是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是
A. 用湿润的pH试纸测稀碱液的pH,测定值偏小
B. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
C. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁红涂料中添加有CuO或FeO中的一种,为探究添加物的成分设计如下实验方案。
(1)请写出实验步骤、预期现象,对应的离子方程式。
(限选试剂:铁粉、3mol/LH2SO4、0.1mol/L酸性KMnO4溶液、10%H2O2、KSCN溶液)

①_____________,②_____________,_____________,③___________,_____________
④操作步骤③中反应的离子方程式为____________。
(2)经分析该铁红涂料中有FeO,为测定铁红中铁的质量分数,兴趣小组的同学称量11.6g该铁红涂料进行了如下实验。
已知:气体由草酸晶体受热分解得到:H2C2O4·2H2O ![]() CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。
CO2↑+CO↑+3H2O。且除铁红外所用试剂均过量。

①装置A、B中的试剂依次是_____、______。
②气体通入后,接下来的操作是____,然后对C装置加热。
③实验前后称得D装置增重8.8g,则此铁红中铁的质量分数是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属铈(58Ce)常用于制作稀土磁性材料,可应用于制造玻璃、打火石、陶瓷和合金等。已知:Ce4++Fe2+=Ce3+ +Fe3+。下列说法正确的是
A. 可用电解熔融CeO2制取金属铈,铈在阳极生成
B. ![]() 、
、![]() 是同素异形体
是同素异形体
C. 铈的原子核外有58个电子
D. 铈能溶于HI溶液,发生反应的离子方程式为:Ce+4H+=Ce4++2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】28g铜、银合金与一定量某浓度的硝酸溶液反应,金属完全溶解,放出的气体与2.24L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中铜的质量是( )
A.3.2g
B.6.4g
C.12.8g
D.21.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】保护环境是每一个公民的责任。下列做法:
①推广使用无磷洗涤剂;②城市生活垃圾分类处理;③推广使用一次性木质筷子;④推广使用清洁能源;⑤过量施用化肥、农药;⑥推广使用无氟冰箱。其中有利于保护环境的是( )
A.①②④⑤
B.②③④⑥
C.①②④⑥
D.③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com