
| A. | 25℃ | B. | 1.01×103Pa | C. | 101kPa | D. | 0℃ |
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X | 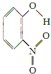 | 0.2 | 45 | 100 |
| Y | 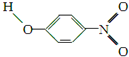 | 1.7 | 114 | 295 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2的水溶液能导电,所以SO2是电解质 | |
| B. | BaSO4难溶于水,其水溶液的导电能力极弱,所以BaSO4是弱电解质 | |
| C. | 液溴不导电,所以液溴是非电解质 | |
| D. | HI熔融状态不能导电,但HI是强电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度(mg/L) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度(mg/L) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2中含有的氢原子数为2NA | |
| B. | 22.4L氧气所含的氧原子数为2NA | |
| C. | 常温常压下,28g氮气所含的分子数为2NA | |
| D. | 2g氢气所含的氢原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3•H2O?NH+4+OH- | B. | KClO3=K++Cl-+3O2- | ||
| C. | H2CO3=2H++CO32- | D. | Ba(OH)2=Ba2++OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com