
 H++OH-△H>0,下列叙述正确的是( )
H++OH-△H>0,下列叙述正确的是( )| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.由水电离出的c(H+)=1×10-12mol/L的溶液pH一定为12 |
| D.将水加热,Kw增大,pH也不变 |
 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源:不详 题型:单选题
| A.V1>V2>V3 | B.V1<V2=V3 |
| C.V1<V2<V3 | D.V1=V2<V3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.1×10 mol/L mol/L | B.1×10 mol/L mol/L | C.1×10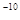 mol/L mol/L | D.1×10 mol/L mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 H =" +206.2" kJ·mol-1
H =" +206.2" kJ·mol-1 H =" +247.4" kJ·mol-1
H =" +247.4" kJ·mol-1 (电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极排出液中含有大量的碳酸盐成份,则阳极的电极反应式为_______,每消耗1mol尿素需要补充______mol氢氧化钾。
(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极排出液中含有大量的碳酸盐成份,则阳极的电极反应式为_______,每消耗1mol尿素需要补充______mol氢氧化钾。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 、
、 的NaOH溶液和
的NaOH溶液和 、
、 的
的 溶液相混合,下列关于该混合溶液的叙述错误的是
溶液相混合,下列关于该混合溶液的叙述错误的是 A.若 ,则一定是 ,则一定是  |
B.在任何情况下都是 |
C.当pH=7时,若 ,则一定是 ,则一定是 |
D.若  , , ,则 ,则  |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(NH)相等的(NH4)2SO4溶液、(NH4)2Fe(SO4)2溶液和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B.0.1 mol·L-1的CH3COOH溶液加水稀释,溶液中c(OH-)减小 |
| C.0.2 mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
| D.0.2 mol·L-1的NaHCO3溶液中c(H+)+c(H2CO3)=2c(CO)+c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com