
 ,则两者的关系正确的是
,则两者的关系正确的是| A.Vb﹤10Va | B.Va ﹥ 10Vb | C.Vb﹥ 10Va | D.Va ﹤10Vb |
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ | C.②③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
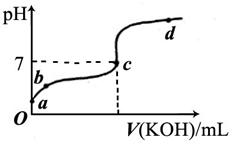
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(OH-) | B.c(NH4+) | C.c(NH3·H2O) | D.c(NH4+)/c(NH3·H2O) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. c(CH3COOH) | B.c(H+) | C.c(OH-) | D.c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.醋酸溶液的导电性比盐酸弱 |
| B.醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 |
| C.0.1mol L-1的CH3COOH溶液中氢离子浓度约为0.001 mol L-1 |
| D.醋酸溶液用水稀释后,氢离子浓度下降 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成了一种强酸弱碱盐 |
| B.等浓度的强酸和弱碱溶液反应 |
| C.浓的强酸和稀的强碱溶液反应 |
| D.浓的弱酸和稀的强碱溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com