
【题目】“化学是一门中心学科,与社会、生活、科研密切的关系。”下列叙述中,不正确的是
A.大量使用燃煤发电是形成雾霾的主要原因
B.天然气、煤气大量泄漏遇到明火会爆炸
C.利用化学反应可实现12C到14C的转化
D.晶体硅可用于光伏发电、制造芯片
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素是所有原子中半径最小的原子;B元素的最高价氧化物对应水化物与其氢化物生成一种盐X;D与A同主族,且与E同周期;E元素的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素中,每一种都与C元素形成原子个数比不相同的化合物.
请回答下列问题:
(1)C和E两元素相比较,非金属性较强的是(填元素名称),可以验证该结论的是(填写编号);
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(2)写出C、D两元素形成的原子个数比为1:1的化合物与E、C两元素形成的原子个数比为1:2的化合物反应的化学方程式: .
(3)A、C、D、E四种元素可形成两种酸式盐,两种酸式盐相互反应的离子方程式为
(4)A和E,A和C可形成甲、乙两种微粒,它们均为负一价双原子阴离子,且甲有18个电子,乙有10个电子,则甲与乙反应的离子方程式为;
(5)B元素的气态氢化物和其一种常见氧化物(双原子分子)能反应生成B的单质,该反应中氧化产物与还原产物的物质的量之比为 .
(6)在火箭推进器中装有液态B2A4和液态A2C2 , 已知0.4mol.液态B2A4和足量液态A2C2反应,生成气态B2和气态A2C,放出256.6kJ的热量.试写出该反应的热化学方程式: . B2A4的电子式
(7)A2C的沸点比A2E 沸点 , 原因是
(8)下列事实可以用氢键解释的是
A.水比硫化氢稳定.
B.氨气易液化.
C.氨气极易溶于水.
D.水结成冰,密度减小,体积增大.
(9)用电子式表示氯化氢的形成过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)SO2气体为无色气体,有强烈刺激性气味,大气主要污染物之一,具有一定的还原性,探究SO2气体还原Fe3+、I2,可以使用的药品和装置如下图所示:
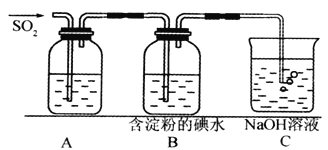
(1)若要从FeCl3溶液中提取晶体,在必须进行的实验操作步骤中,没有用到的玻璃仪器有________________(填字母)。
a.酒精灯 b.烧瓶 c.漏斗 d.烧杯 e.玻璃棒
(2)装置A中的现象是__________________,写出B中发生反应的离子方程式:__________________。
(3)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,取A中的溶液,分成两份,并设计了如下试验
方案①:向第一份溶液中加入少量酸性KMnO4溶液,紫红色褪去。
方案②:向第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案中不合理的是_______________(填序号)。
(Ⅱ)SO2溶于水生成亚硫酸,亚硫酸的酸性强于次氯酸。选择下面的装置和药品来探究亚硫酸与次氯酸的酸性强弱。
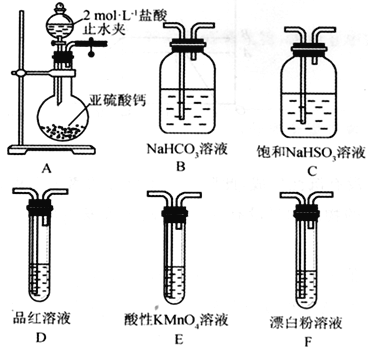
(4)装置正确的连接顺序为A、________________________________、D、F,其中装置B的作用是_________。证明亚硫酸的酸性强于次氯酸的现象为_____________________________。
(Ⅲ)某同学对SO2与漂粉精的反应进行了实验探究。
操作 | 现象 |
取4 g漂粉精固体,加入100 mL水 | 部分固体溶解,溶液略有颜色 |
过滤,测漂粉精溶液的pH | pH试纸先变蓝(约为12),后褪色 |
| ①溶液出现浑浊,并变为黄绿色 ②稍后,产生大量白色沉淀,黄绿色褪去 |
(5)C12和Ca(OH)2反应制取漂粉精的化学方程式是______________________________________。
(6)pH试纸颜色的变化说明漂粉精溶液具有的性质是__________________________________。
(7)现象①中溶液变为黄绿色的可能原因:随溶液酸性的增强,漂粉精的有效成分ClO-和Cl-发生反应。写出漂粉精在酸性条件下发生反应的离子方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与图像对应符合的是( )

A. 对于达到平衡状态的N2(g)+3H2(g)![]() 2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
2NH3(g)在t0时刻充入了一定的NH3,平衡逆向移动
B. 对于反应2X(g)+3Y(g)![]() 2Z(g) ΔH<0,y可以表示Z的百分含量
2Z(g) ΔH<0,y可以表示Z的百分含量
C. 该图像表示的方程式为2A=B+3C
D. p2>p1,T1>T2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
①元素电负性越大表示该元素的金属性越强 ②元素电负性越大表示该元素的非金属性越强 ③元素电负性很小表示该元素的单质不发生化学反应 ④元素电负性很大表示该元素的单质在发生化学反应时一般易得到电子
A.①③B.①④C.②③D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJmol﹣1表示.请认真观察如图,然后回答问题. 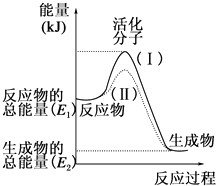
(1)图中所示反应是(填“吸热”或“放热”)反应.
(2)已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由1mol氢气和1mol 碘反应生成HI会(填“放出”或“吸收”)kJ的热量.在化学反应过程中,是将转化为 .
(3)下列反应中,属于放热反应的是 , 属于吸热反应的是 .
①物质燃烧
②炸药爆炸
③酸碱中和反应
④二氧化碳通过炽热的碳
⑤食物因氧化而腐败
⑥Ba(OH)28H2O与NH4Cl反应
⑦铁粉与稀盐酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式正确的是( )
A. 醋酸溶于水:CH3COOH===CH3COO-+H+
B. NaHSO4溶于水:NaHSO4===Na++HSO4-
C. 碳酸氢钠溶于水:NaHCO3![]() HCO
HCO![]() +Na+
+Na+
D. 次氯酸溶于水:HClO![]() H++ClO-
H++ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是( )
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是( )
A. 1 mol LiAlH4在125℃完全分解,转移3 mol电子
B. LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
C. LiAlH4溶于水得到无色溶液,化学方程式可表示为:LiAlH4 + 2H2O![]() LiAlO2 + 4H2↑
LiAlO2 + 4H2↑
D. LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
B. 乙烷和乙烯都能使酸性KMnO4溶液褪色
C. 植物油和动物脂肪都不能使溴水褪色
D. 乙醇和乙酸都能与金属钠反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com