
| A. | 镀锌铁制品,镀层破损后铁制品将彻底失去保护 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1,可知单质B比单质A稳定 | |
| C. | 草木灰与铵态氮肥混合施用效果更好 | |
| D. | Na2CO3可做食用碱,NH4Cl溶液可去除铁锈 |
分析 A.镀锌铁制品破损后,活泼性较强的锌作原电池的负极,活泼性较弱铁作原电池的正极,铁被保护;
B.能量越低越稳定;
C.草木灰显碱性,与铵态氮肥混合会反应产生氨气,降低了施肥效果;
D.Na2CO3水解显碱性,NH4Cl水解显酸性.
解答 解:A.镀锌铁制品破损后,活泼性较强的锌作原电池的负极,活泼性较弱铁作原电池的正极,铁被保护,故A错误;
B.由A转化为B时△H═+119 kJ•mol-1,说明这个过程是吸热反应,反应物能量低,生成物能量高,即B的能量高,能量越低越稳定,A稳定,故B错误;
C.草木灰显碱性,与铵态氮肥混合会反应产生氨气,降低了施肥效果,故C错误;
D.Na2CO3水解显碱性可做食用碱,NH4Cl水解显酸性可去除铁锈,故D正确;
故选D.
点评 本题考查了金属的电化学腐蚀与防护、化学反应与能量、盐类水解的应用,培养了学生化学学科素养,体现了利用化学服务于生活的重要性.


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{W}{A+16}$(A-N+8)mol | B. | $\frac{W}{A+16}$(A-N+10)mol | C. | (A-N+8)mol | D. | $\frac{W}{A+16}$(A-N+6)mol |
查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
生产生活中的许多现象或应用都与化学知识有关。下列现象或应用与胶体性质无关的是
A.将盐卤或石膏加入豆浆中,制成豆腐
B.冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
C.泡沫灭火器中将Al2(SO4)3与NaHCO3两溶液混合后,喷出大量泡沫,起到灭火作用
D.胶体、溶液和浊液这三种分散系的根本区别是分散质粒子直径的大小
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2-、F-、Na+、Mg2+ | B. | Na+、Mg2+、S2-、Cl- | ||
| C. | F-、Cl-、Br-、I- | D. | Na+、Mg2+、K+、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2既是氧化剂又是还原剂 | |
| B. | FeCl3对H2O2的分解起催化作用 | |
| C. | 使用FeCl2代替FeCl3,不能起到催化作用 | |
| D. | 反应过程中有Fe2+生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KClO3在反应中是还原剂 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应,有 2mol 电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C12与水反应 C12+H2O═2 H++C1-+ClO- | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 少量金属钠放入冷水中:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 碳酸氢钠溶液与足量盐酸反应:HCO3-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
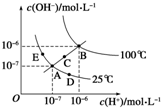
| A. | 图中五点Kw的关系:B>C>A=D=E | |
| B. | 若从A 点到D 点,可采用:温度不变向水中加入少量的酸 | |
| C. | 若从A 点到C 点,可采用:温度不变向水中加入适量的NH4Cl 固体 | |
| D. | 若处在B 点时,将pH=2 的硫酸与pH=10 的KOH 溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上第二次模拟化学试卷(解析版) 题型:选择题
关于下列各图的叙述,正确的是( )

A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6Kj•mol﹣1
B.乙表示恒温恒容条件下发生的可逆反应2NO2 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com