
| A. | H2O2既是氧化剂又是还原剂 | |
| B. | FeCl3对H2O2的分解起催化作用 | |
| C. | 使用FeCl2代替FeCl3,不能起到催化作用 | |
| D. | 反应过程中有Fe2+生成 |
分析 将FeCl3加入到H2O2溶液中,把K3Fe(CN)6溶液滴加到上述溶液中呈现蓝色,可知发生H2O2+2Fe3+=2Fe2++O2↑+2H+、H2O2+2Fe2++2H+=2Fe3++2H2O、Fe2+与K3Fe(CN)6反应生成蓝色的KFeFe(CN)6,以此来解答.
解答 解:A.由现象可知,发生总反应为2H2O2═O2↑+2H2O,H2O2既是氧化剂又是还原剂,故A正确;
B.H2O2+2Fe3+=2Fe2++O2↑+2H+、H2O2+2Fe2++2H+=2Fe3++2H2O,FeCl3作催化剂,故B正确;
C.使用FeCl2代替FeCl3,可发生H2O2+2Fe2++2H+=2Fe3++2H2O,能作催化剂,故C错误;
D.发生2Fe3++H2O2═2Fe2++O2+2H+,可知反应过程中有Fe2+生成,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化、信息中亚铁离子的性质为解答的关键,注意总反应的判断,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:实验题


查看答案和解析>>
科目:高中化学 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:选择题
已知甲、乙、丙、丁是中学化学常见的物质,一定条件下可发生如下转化: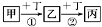 ,下列相关离子方程式或化学方程式错误的是
,下列相关离子方程式或化学方程式错误的是
A. ①可能为AlO2-+H++H2O=Al(OH)3↓
B. ①可能为Fe+2Fe3+=3Fe2+
C. ②可能为2NO+O2=2NO2
D. ②可能为Na2CO3+H2O+CO2=2NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸的结构简式:C2H4O2 | B. | MgCl2的电子式: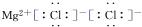 | ||
| C. | 中子数为8的碳原子:${\;}_{6}^{8}$C | D. | F-的结构示意图: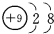 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀锌铁制品,镀层破损后铁制品将彻底失去保护 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1,可知单质B比单质A稳定 | |
| C. | 草木灰与铵态氮肥混合施用效果更好 | |
| D. | Na2CO3可做食用碱,NH4Cl溶液可去除铁锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O).下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O).下列说法正确的是( )| A. | 该装置将化学能转化为光能和电能 | |
| B. | b电极的反应为:2H2O-4e-═O2↑+4H+ | |
| C. | 每生成1 mol O2,有44 g CO2被还原 | |
| D. | a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com