
根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4… |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO | Cl2、Mn2+… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1∶2
C.第③组反应中生成1 mol Cl2,转移电子2 mol
D.氧化性由强到弱顺序为MnO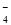 >Cl2>Fe3+>Br2
>Cl2>Fe3+>Br2
D
【解析】
试题分析:A、根据氧化还原反应理论,过氧化氢作还原剂,被氧化的产物是氧气,根据元素守恒,产物中含有水生成,正确;B、氯气与溴化亚铁反应,当产物中含有铁离子、氯离子、溴离子时,说明氯气不足,氯气只与亚铁离子反应,所以氯气与溴化亚铁的物质的量之比是1:2,正确;C、高锰酸根离子与氯离子反应生成氯气和锰离子,若生成1mol氯气,则转移电子的物质的量是2mol,正确;D、从以上的事实可以判断,氯气先氧化亚铁离子,说明亚铁离子的还原性比溴离子强,也即铁离子的氧化性比溴单质弱,所以氧化性由强到弱顺序为MnO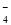 >Cl2> Br2 >Fe3+,错误,答案选D。
>Cl2> Br2 >Fe3+,错误,答案选D。
考点:考查对氧化还原反应产物的判断,氧化还原反应规律的应用


科目:高中化学 来源:2015届河北省邯郸市高三第一次调研考试化学试卷(解析版) 题型:选择题
为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是( )
序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
① | KNO3溶液 | KOH | 滴入稀HNO3同时用pH计测定至溶液呈中性 |
② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
A.①②③ B.②③④
C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2015届河北省“五个一名校联盟”高三教学质量监测(一)化学试卷(解析版) 题型:选择题
粒子甲与粒子乙在溶液中的转化关系如下图所示,粒子甲不可能是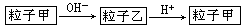
A.NH4+ B.Al C.HCO3一D.SO2
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:推断题
(12分)对溴甲苯是合成农药溴螨酯的重要原料。工业用液溴、甲苯与1-丙醇共热合成对溴甲苯和1-溴丙烷,其原子利用率很高。实验室模拟的合成流程和相关数据如下:已知:甲苯与溴在有水存在时能反应。
物质 | 甲苯 | 1-丙醇 | 1-溴丙烷 |
沸点℃ | 110.8 | 97.2 | 71 |
物质 | 对溴甲苯 | 邻溴甲苯 | |
沸点℃ | 184.3 | 181.7 | |
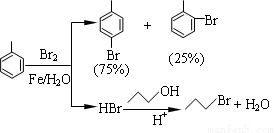
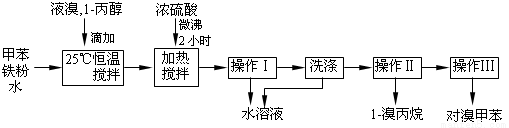
(1)液溴的颜色是__ __ __,实验室存放液溴时应密闭保存,同时需要在试剂瓶中加__ ___,以减少挥发。
(2)25℃恒温搅拌至溴的颜色完全褪去时完成甲苯的溴代反应。搅拌的目的是__________。加入水的作用是:易于控制温度;____________________。
(3)加热搅拌操作中加入浓硫酸,搅拌,完成1-丙醇的取代反应,加入浓硫酸的作用是___ ___,加热微沸2小时的目的是_______ _____。
(4)操作Ⅰ的名称是___________,洗涤操作应在_________(填写仪器名称)中进行。
(5)经以上分离操作后,粗对溴甲苯中还含有的最主要杂质为________(填写名称),使用操作Ⅱ分离出1-溴丙烷的原理是______________________________________。
(6)分离出的水溶液中含HBr、H2SO4和Fe3+离子,将水溶液稀释定容至1000mL,取20.00mL,加入几滴甲基橙作指示剂,用一定浓度的NaOH溶液滴定,测定出HBr的物质的量明显低于理论值,原因是_____________________;有同学认为无需加入指示剂,也能完成滴定,提出这一观点的理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
用Na2SO3溶液吸收硫酸工业尾气中的二氧化硫,将所得的混合液进行电解循环再生,这种新 工艺叫再生循环脱硫法。其中阴、阳离子交换膜组合循环再生机理如下图所示,则下列有关说法中不正确 的是( )
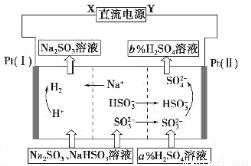
A.X为直流电源的负极,Y为直流电源的正极
B.阳极区pH增大
C.图中的b>a
D.该过程中的产品主要为H2SO4和H2
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
下列各项叙述中不正确的是( )
A.10 ℃ 时NaCl溶解度为35.7g,则此时饱和NaCl 溶液的质量分数小于35.7 %
B.向Na2CO3溶液中加入少量NaHCO3 固体,溶液pH 减小
C.50mL 1.0 mol·L-1盐酸与60 mL 1.0 mol·L-1盐酸分别跟50 mL 1.1 mol·L-1NaOH溶液进行反应,中和热数值不相等
D.一定条件下,向水中加入少量NaHSO4,可使水的电离程度减小
查看答案和解析>>
科目:高中化学 来源:2015届河北正定中学上学期高三第一次考试化学试卷(解析版) 题型:选择题
有关化学用语的表达正确的是( )
A.Na2O2电子式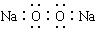 B.二氧化硅的分子式SiO2
B.二氧化硅的分子式SiO2
C.乙烯的结构简式CH2CH2D.硫原子的最外层电子排布式3s23p4
查看答案和解析>>
科目:高中化学 来源:2015届江西省高三暑期化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.少量金属钠加到冷水中:Na+2H2O===Na++2OH-+H2↑
B.NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH-+HCO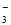 ===CaCO3↓+H2O
===CaCO3↓+H2O
C.硫酸铝溶液中加入过量氨水:Al3++4NH3·H2O===AlO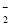 +4NH
+4NH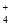 +2H2O
+2H2O
D.将2 mol/L AlCl3溶液和7 mol/L NaOH溶液等体积混合:2Al3++7OH-===Al(OH)3↓+ AlO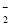 +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届江西省第一学期高三第一次月考化学(A卷)试卷(解析版) 题型:选择题
常温,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中: I-、NO3-、SO42-、Na+
B.由水电离的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、K+、Cl-、HCO3-
C.c(H+)/c(OH-)=1012的溶液中: NH4+、Al3+、NO3-、Cl-
D.c(Fe3+)=0.1 mol·L-1的溶液中:K+、ClO-、SO42-、SCN-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com