
【题目】ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法不正确的是
A. KClO3在反应中得到电子 B. ClO2是还原产物
C. H2C2O4发生氧化反应 D. 1 molKClO3参加反应有2mol电子转移
【答案】D
【解析】
反应2KClO3+H2C2O4+H2SO4![]() 2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价由+5降低为+4价,C元素的化合价由+3升高到+4价,以此来解答。
2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价由+5降低为+4价,C元素的化合价由+3升高到+4价,以此来解答。
A.因反应中Cl元素的化合价由+5降低为+4价,则KClO3在反应中得到电子,A正确;
B.Cl元素的化合价降低,被还原,对应的产物为还原产物,即ClO2是还原产物,B正确;
C.因C元素的化合价由+3升高到+4价,则H2C2O4在反应中作还原剂,被氧化,发生氧化反应,C正确;
D.Cl元素的化合价由+5降低为+4价,1molKClO3参加反应转移的电子为1mol×(5-4)=1mol,D错误;
答案选D。


 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组为研究氯气的性质并模拟工业制备漂白粉,设计了下列装置进行实验。已知:
①A 中反应为 KClO3+6HCl(浓) = KCl+3Cl2↑+3H2O;
②石灰乳的主要成分为 Ca(OH)2,其他杂质不参与反应。
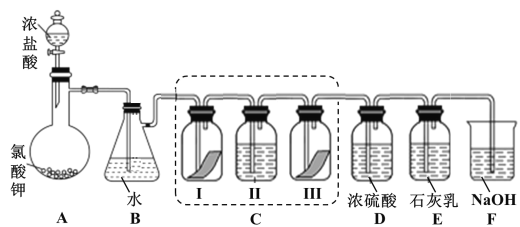
(1)写出 B 装置中反应的化学方程式_______________。实验结束后,立即将 B 中溶液滴几滴在紫色石蕊试纸上,可观察到的现象是______________
(2)装置 C 的实验目的是验证氯气是否具有漂白性,为此 C 中 I、II、III 处依次放入的物质正确的是_________(填编号)。
编号 | I | II | III |
A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
B | 干燥的有色布条 | 浓硫酸 | 湿润的有色布条 |
C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
D | 湿润的有色布条 | 碱石灰 | 干燥的有色布条 |
(3)待 E 中物质完全反应后,经过一系列加工处理,得到漂白粉样品,其主要成份为_________、____________(填化学式)。
(4)F 装置的作用是(用离子方程式表示)_____________
(5)为测定(3)中所得漂白粉的有效成份含量。称取 a g 漂白粉样品溶解,往所得溶液中通入 CO2 至不再产生沉淀为止,该过程的化学方程式为_____________。若反应生成沉淀的物质的量为 b mol,则该漂白粉中有效成份的质量分数为_________________(用含 a、b 的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 1L0.1mol/LFeCl3溶液最多可形成胶体粒子数为0.1NA
B. 100mL98%(p=1.84g/mL)硫酸与足量铜共热,充分反应后转移的电子数为1.84NA
C. 4.0gH218O与D2O的混合物中所含质子数一定为2NA
D. 标准状况下,2.24L苯中含有的碳碳键数为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AgCl的沉淀溶解平衡为AgCl(s)![]() Ag+(aq)+Cl(aq),下列说法中错误的是()
Ag+(aq)+Cl(aq),下列说法中错误的是()
A. 加入水后溶解平衡不移动
B. AgCl饱和溶液中c(Ag+)=![]() mol/L
mol/L
C. 用NaCl溶液代替蒸馏水洗涤AgCl沉淀,可以减少沉淀损失
D. 反应AgCl+NaBr=AgBr+NaCl易进行,说明溶解度:AgCl>AgBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性:Z>W>X
C. 四种元素的单质中,Z单质的熔、沸点最低
D. W的单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2molNaOH和0.1molCa(OH)2的溶液中持续稳定地通入CO2气体,当通入气体为6.72L(标准状况)时立即停止,则这一过程中,溶液中离子数目和通入CO2气体的体积关系正确的图像是(气体的溶解忽略不计)
A. 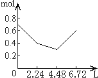 B.
B. 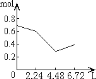
C. 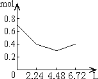 D.
D. 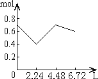
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机化合物A、B、C、D、E存在如图所示转化关系,且C能跟NaHCO3发生反应,C和D的相对分子质量相等,E为无支链的化合物.
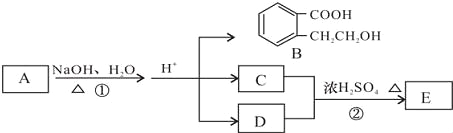
请回答下列问题:
(1)已知E的相对分子质量为102,其中碳、氢两种元素的质量分数分别为58.8%、9.8%,其余为氧,则E的分子式为 .
(2)B在一定条件下可以发生缩聚反应生成某高分子化合物,此高分子化合物的结构简式为 ![]() .
.
(3)D也可以由溴代烃F在NaOH溶液中加热来制取,写出此反应的化学方程式 .
(4)反应①的化学方程式 .
(5)B有多种同分异构体,请写出一种同时符合下列四个条件的结构简式: .
a.能够发生水解
b.能发生银镜反应
c.能够与FeCl3溶液显紫色
d.苯环上的一氯代物只有一种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国研究锂硫电池获得突破,电池的总反应是16Li+S8 ![]() 8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
8Li2S ,充放电曲线如图所示,下列说法不正确的是( )
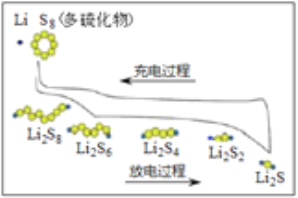
A. 充电时,电能转化为化学能
B. 放电时,锂离子向正极移动
C. 放电时,1mol Li2S6转化为Li2S4得到2mole-
D. 充电时,阳极总电极反应式是8S2- -16e- = S8
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com