
| A. | c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) | B. | c(HAc)>c(CH3COO-) | ||
| C. | 2c(H+)=c(CH3COO-)-c(CH3COOH) | D. | c(CH3COOH)+c(CH3COO-)=0.02mol/L |
分析 把0.02 mol/LCH3COOH溶液和0.01 mol/L NaOH溶液以等体积混合,两溶液反应后的得到等浓度的为CH3COOH和CH3COONa,
A.根据混合液中的物料守恒、电荷守恒判断;
B.CH3COOH的电离程度大于CH3COO-的水解程度,则c(CH3COO-)>c(CH3COOH);
C.结合A的分析结果判断;
D.根据混合液中的物料守恒判断.
解答 解:把0.02 mol/LCH3COOH溶液和0.01 mol/L NaOH溶液以等体积混合,两溶液反应后的得到等浓度的为CH3COOH和CH3COONa,
A.溶液中存在物料守恒:c(CH3COOH)+c(CH3COO-)=2c(Na+),电荷守恒:c(OH-)+c(CH3COO-)=c(Na+)+c(H+),二式联立可得:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),故A正确;
B.醋酸与醋酸钠的物质的量浓度相等,由于CH3COOH的电离程度大于CH3COO-的水解程度,则c(CH3COO-)>c(CH3COOH),故B错误;
C.根据A可知:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-),故C错误;
D.两溶液等体积混合,体积扩大一倍,浓度为原来的二分之一,根据物料守恒可得:c(CH3COOH)+c(CH3COO-)=0.01mol/L,故D错误;
故选A.
点评 本题考查了离子浓度大小比较,题目难度中等,明确反应后溶质组成为解答关键,注意掌握电荷守恒、物料守恒及盐的水解原理的含义及应用,试题培养了学生的分析能力及灵活应用能力.


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 向0.1 mol•L-1的醋酸溶液中加水或通入HCl气体都能使$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大 | |
| B. | 0.1 mol•L-1的醋酸钠溶液20 mL与0.1 mol•L-1盐酸10 mL混合后溶液显酸性,则有c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | |
| C. | 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c (Na+)═c (SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| D. | 0.1 mol•L-1某一元酸HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,则该溶液中由水电离出的c(H+)=1×10-11mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
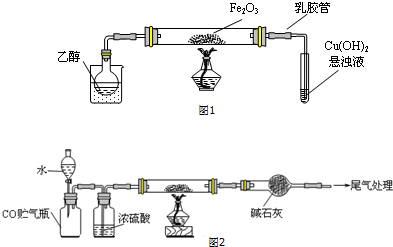
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
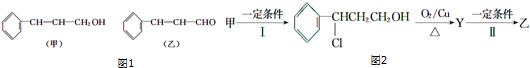
| 分子式 | C16H14O2 |
| 部分性质 | 能使Br2/CCl4褪色 |
| 能在稀H2SO4中水解 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
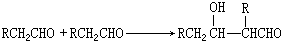
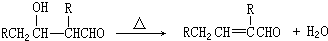

 F:
F: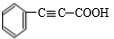

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | [Cl-]>[NH4+]>[H+]>[OH-] | B. | [Cl-]>[H+]>[NH4+]>[OH-] | C. | [NH4+]>[OH-]>[Cl-]>[H+] | D. | [OH-]>[H+]>[Cl-]>[NH4+] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L H2O含有NA个分子 | |
| B. | 1L 1mol•L -1的NaClO 溶液中含有ClO-的数目少于NA个 | |
| C. | 0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子 | |
| D. | 0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
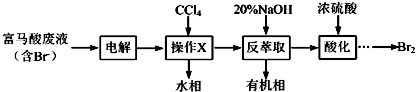
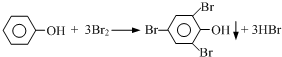
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com