
| A�� | �ڵ������Һ��ע��һ�������������ʹ��Һ�ָ���ԭʼ״̬ | |
| B�� | �ڵ������Һ��ͨ������4.48L���Ȼ������岢ע��0.1mol��ˮ����ʹ��Һ�ָ���ԭʼ״̬ | |
| C�� | ������������������ʵ���������������������ʵ�����0.75�� | |
| D�� | ���������������ƽ��Ħ������Ϊ58g/mol |
���� ��ʯī�缫����Ȼ�����Һ���������ϲ��������������������ƣ��������ϲ������������Լ�����������ʸ�ԭ�ķ����ǣ���ʲô��ʲô�����ݵ��صĹ���ԭ�����ش��жϣ�
��� �⣺A������Ȼ��Ʋ����������������������ƣ��ڵ������Һ��ͨ��HCl�������ʹ��Һ�ָ���ԭʼ״̬����A����
B�����0.1mol•L-1��NaCl��Һ��ͨ��һ��ʱ����������ռ����������֮��Ϊ4��3����ʱ�������ϲ��������������������������ϲ�������������ͭ�Ȼ��⡢����ˮ����ʹ����ʸ�ԭ�����Dz�֪����Һ�����������������������B����
C���������ϲ��������������������������ϲ�������������������������������ȵģ������ռ����������֮��Ϊ4��3��������Ϊ�Dz�����������������3mol��������1mol�������������������������ʵ��������������������������������ʵ�����0.75������C��ȷ��
D�������ϲ����������������������ʵ���֮����3��1�������������ƽ��Ħ������Ϊ$\frac{71g/mol��3+32g/mol��1}{4mol}$=61.25g/mol����D����
��ѡC��
���� ���⿼��ѧ�����صĹ���ԭ���Լ�Ӧ��֪ʶ��ע��֪ʶ��Ǩ��Ӧ���ǹؼ����Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CCl2F2 | B�� | 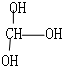 | C�� | CH3CH2OH | D�� | 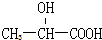 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ���ռʳ�� | B�� | ���������ᡢ��ʯ�� | ||
| C�� | Һ�ȡ����ᡢ���� | D�� | �ɱ���ʯ��ʯ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ij��Ӧ���̣�������ϵ��ʼ̬ΪS����̬ΪL������֮��ı仯�����λ��ߣ���������������Ŀ���м䲽�裩������ͼ��ʾ����������
ij��Ӧ���̣�������ϵ��ʼ̬ΪS����̬ΪL������֮��ı仯�����λ��ߣ���������������Ŀ���м䲽�裩������ͼ��ʾ����������| A�� | һ���С�H1��0 | B�� | һ���С�H2��0 | ||
| C�� | һ���С�H1��0����H2��0 | D�� | һ���С�H1+��H2=0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ����Ϊ�����Ƶá����Ӳ����������ʵ�װ�ã����ȼ��г�����ʡ�ԣ���������Ʋ��ܴﵽĿ���ǣ�������
��ͼ����Ϊ�����Ƶá����Ӳ����������ʵ�װ�ã����ȼ��г�����ʡ�ԣ���������Ʋ��ܴﵽĿ���ǣ�������| ѡ�� | ���� | װ����ҩƷ | ||
| a | b | C | ||
| A | C2H2 | ����ʳ��ˮ+��ʯ | CuSO4��Һ | ��ˮ |
| B | CO2 | ϡ����+ʯ��ʯ | ����NaHCO3��Һ | ���ӵ���Һ |
| C | C2H4 | ������+NaOH�Ҵ���Һ | ˮ | K2Cr2O7������Һ |
| D | SO2 | ̼+Ũ���� | ������ˮ | Ʒ����Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D |
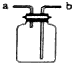 | 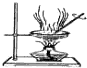 | 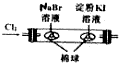 | 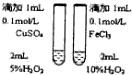 |
| �ø�װ���ſ������ռ�H2��CO2��Cl2������ | ����AlCl3������Һ�Ʊ�AlCl3���� | ����֤��������Cl2��Br2��I2 | �Ƚϲ�ͬ�����Է�Ӧ���ʵ�Ӱ�� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
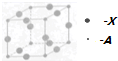 A��B��C��D��X����Ԫ�ص�ԭ���������ε�����A��B�ij��������ǹ��ɿ�������Ҫ�ɷ֣�C �Ļ�̬ԭ�Ӻ������ռ��7���������ֻ��1��δ�ɶԵ��ӣ�D�Ļ�̬ԭ�ӵ�M�ܲ���ֻ��1�ԳɶԵ��Ӻ�2��δ�ɶԵ��ӣ�XԪ�ش��ڵ������ڢ�B�壮
A��B��C��D��X����Ԫ�ص�ԭ���������ε�����A��B�ij��������ǹ��ɿ�������Ҫ�ɷ֣�C �Ļ�̬ԭ�Ӻ������ռ��7���������ֻ��1��δ�ɶԵ��ӣ�D�Ļ�̬ԭ�ӵ�M�ܲ���ֻ��1�ԳɶԵ��Ӻ�2��δ�ɶԵ��ӣ�XԪ�ش��ڵ������ڢ�B�壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 NO2��O2������KNO3������ȼ�ϵ�أ���ԭ����ͼ��ʾ���õ���ڷŵ������ʯīI�缫������������Y��Y��ѭ��ʹ�ã�����˵����ȷ���ǣ�������
NO2��O2������KNO3������ȼ�ϵ�أ���ԭ����ͼ��ʾ���õ���ڷŵ������ʯīI�缫������������Y��Y��ѭ��ʹ�ã�����˵����ȷ���ǣ�������| A�� | O2��ʯī������������Ӧ�ŵ�ʱ��NO3-��ʯī��缫Ǩ�� | |
| B�� | ʯī���������ķ�Ӧ��NO+O2+e-=NO3 | |
| C�� | ��ص��ܷ�ӦʽΪ��4NO2+O2=2N2O5 | |
| D�� | �����·ͨ��4mole-�������Ϲ�����2molN2O5 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com